
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |

分析 (1)H2O2作氧化剂的反应产物为水,不会引入新的杂质;根据表中数据可知Fe3+比Fe2+容易转化为沉淀;加入的物质用于调节pH以除去杂质,且不能引入新杂质,先根据溶液的pH计算氢离子浓度,再结合水的离子积常数计算氢氧根离子浓度,最后根据c(Fe3+)=$\frac{Ksp[Fe(OH)_{3}]}{{c}^{3}(O{H}^{-})}$计算铁离子浓度;
(2)依据碘化钾和氯化铜发生氧化还原反应,生成碘化亚铜沉淀,和碘单质,碘单质遇淀粉变蓝,依据碘单质被Na2S2O3标准溶液滴定到终点,发生反应离子方程式计算分析.
解答 解:(1)H2O2作氧化剂的反应产物为水,不会引入新的杂质,所以最适合作氧化剂X的是H2O2;根据表中数据可知Fe3+比Fe2+容易转化为沉淀,因此要把Fe2+转化为Fe3+,所以加入双氧水的目的是将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离;为得到纯净的CuCl2•2H2O晶体,加入的物质来调节pH且不能引进新的杂质,所以加入物质应能转化为氯化铜,则可以加入CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3;
溶液的pH=4,所以溶液中氢离子浓度为10-4 mol/L,则氢氧根离子浓度为10-10 mol/L,c(Fe3+)=$\frac{Ksp[Fe(OH)_{3}]}{{c}^{3}(O{H}^{-})}$=$\frac{2.6×1{0}^{-39}}{(1×1{0}^{-10})^{3}}$=2.6×10-9mol/L;
故答案为:C;将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离;CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3;2.6×10-9mol/L;
(2)测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.1000mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL;反应的化学方程式为:2Na2S2O3+I2═Na2S4O6+2NaI,
①硫代硫酸钠滴定碘单质,利用碘单质遇淀粉变蓝选择指示剂为淀粉;
故答案为:淀粉溶液;
②CuCl2溶液与KI反应的离子方程式为为:2Cu2++4I-=2CuI↓+I2,
故答案为:2Cu2++4I-=2CuI↓+I2;
③依据2Na2S2O3+I2═Na2S4O6+2NaI,2Cu2++4I-=2CuI↓+I2;
得到 2Na2S2O3~2Cu2+
2 2
0.1000mol/L×0.0200L 0.1000mol/L×0.0200L=0.002mol
试样中CuCl2•2H2O的质量百分数=$\frac{0.002mol×171g/mol}{0.36g}$×100%=95%,
故答案为:95%.
点评 本题考查Ksp计算和物质制备、沉淀溶解平衡的分析应用、滴定实验的原理应用等,为高频考点,侧重于学生的分析、计算能力的考查,把握滴定过程的反应原理和计算方法是解本题的关键,难度较大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | V2O5 | B. | Cr2O3 | C. | MnO2 | D. | Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
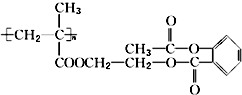 ,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )
,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )| A. | 3 mol | B. | 4 mol | C. | 5 mol | D. | 4n mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| B. | Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | NaHCO3溶液中:c(OH-)+c(H2CO3)=c(H+)+c(CO32-) | |
| D. | 常温下,pH=4.75、浓度均为0.1mol•L-1的CH3COOH和CH3COONa混合液:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl固体 | B. | Zn粉 | C. | SO3固体 | D. | CuSO4晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 没食子儿茶素的结构如图所示,关于该物质下列叙述中正确的是( )
没食子儿茶素的结构如图所示,关于该物质下列叙述中正确的是( )| A. | 分子式为C15H12O5 | |
| B. | 遇FeCl3溶液不发生显色反应 | |
| C. | 1mol该物质与4molNaOH恰好完全反应 | |
| D. | 易发生氧化反应和取代反应,难发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com