
| A. | ①③ | B. | ③⑤ | C. | ③④ | D. | ②⑤ |
分析 水电离产生的H+浓度为1×10-13mol•L-1的溶液,水的电离受到抑制,该溶液可能为酸或碱的溶液,利用离子之间不能结合生成水、气体、沉淀、弱电解质,不能发生氧化还原反应来分析离子在溶液中的共存.
解答 解:因由水电离产生的H+浓度为1×10-13mol•L-1的溶液,小于1×10-7mol•L-1,水的电离受到抑制,该溶液可能为酸或碱的溶液,
①碱溶液中该组离子不反应,但酸溶液中NO3-、S2- 发生氧化还原反应而不能大量共存,故①错误;
②碱溶液中Fe2+、OH-结合生成沉淀,酸溶液中该组离子不反应,故②错误;
③该组离子在酸或碱溶液中都不发生反应,则一定能大量共存,故③正确;
④酸溶液中HCO3-与H+结合生成二氧化碳和水,碱溶液中HCO3-与OH-结合生成碳酸根离子和水,生成的碳酸根离子与Ca2+结合生成碳酸钙沉淀,则一定不能共存,故④错误;
⑤K+、Ba2+、Cl-、NO3-离子在酸或碱溶液中都不发生反应,则一定能大量共存,故⑤正确;
故选B.
点评 本题考查离子的共存问题,题目难度中等,明确水的电离这一信息的利用是解答本题的关键,然后熟悉离子的性质及离子之间的反应即可解答.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D | |
| A | - | - | ↑ | |
| B | - | ↓ | ↓ | |
| C | - | ↓ | - | |
| D | ↑ | ↓ | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 目的 | A.实验室制取并收集O2 | B.检验装置气密性 | C.制取蒸馏水 | D.分离水和四氯化碳 |
| 装置或操作 |  |  | 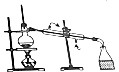 | 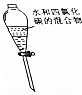 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡正向移动 | B. | 平衡逆向移动 | ||
| C. | 正逆反应速率都增大 | D. | NH3的质量分数增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
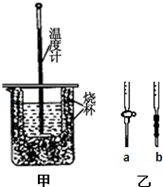 酸碱中和反应是中学化学一类重要的反应,某学生实验小组对课本中的两个酸碱中和实验进行了研究.
酸碱中和反应是中学化学一类重要的反应,某学生实验小组对课本中的两个酸碱中和实验进行了研究.| 实验次数 | 起始滴定管读数 | 终点滴定管读数 |
| 1 | 0.00mL | 24.02mL |
| 2 | 0.50mL | 24.46mL |
| 3 | 2.50mL | 25.02mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl中含有35Cl | |
| B. | 生成物Cl2的平均相对分子质量为73.3 | |
| C. | 1molK35ClO3参加反应,失去电子数为5NA | |
| D. | 氧化剂和还原剂的物质的量之比1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
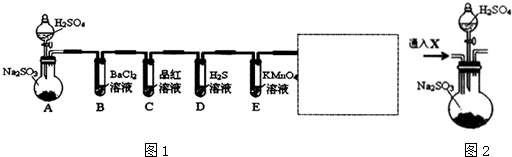
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na+、Ca2+、Cl-、NO3- | B. | Fe2+、H+、SO32-、ClO- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、SCN- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com