
| ѹǿ/MPa �¶�/�� |
0.1 | 0.5 | 1 | 10 | ��ѹΪ1.01x105 =101kPa =0.1MPa |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% | |
| 500 | 93.5% | 96.9% | 97.8% | 98.7% | |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
| 2-2x+1-x+2x |
| 2+1 |
| 11 |
| 15 |
| 0.8mol��2 |
| 2mol |
| c(SO3)2 |
| c(SO2)2?c(O 2) |
| (0.8mol/L)2 |
| (0.2mol/L)2��0.1mol/L |
| 1 |
| 2 |
|
|
|
| 1 |
| 2 |
| 1 |
| 2 |
|
| 1 |
| 2 |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ʵ�鲽�� | ʵ����� | Ԥ������ͽ��� |
| ��һ�� | ȡ������Ʒ��ĩ�ڵ��Թ��У���������� 2mol/LNaOH��Һ�����������Թ� ȡ������Ʒ��ĩ�ڵ��Թ��У���������� 2mol/LNaOH��Һ�����������Թ� |
�Թ��й�����٣���Һ��ɫ �Թ��й�����٣���Һ��ɫ |
| �ڶ��� | װ��ù���װ�ã������Թ��е���Һ����Һ�������ֱ����ڲ�ͬ�Թ��б��� װ��ù���װ�ã������Թ��е���Һ����Һ�������ֱ����ڲ�ͬ�Թ��б��� |
---- ---- |
| ������ | ȡ������������Թ��У�����1mol/Lϡ���ᣬ�������е���2��3��10%KSCN��Һ ȡ������������Թ��У�����1mol/Lϡ���ᣬ�������е���2��3��10%KSCN��Һ |
������KSCN��Һ����Һ��죬��˵�������к���Fe2O3 ������KSCN��Һ����Һ��죬��˵�������к���Fe2O3 |
| ���IJ� | ȡ��Һ��ε���1mol/Lϡ����ֱ���Թ������������е���Ũ��ˮֱ������ ȡ��Һ��ε���1mol/Lϡ����ֱ���Թ������������е���Ũ��ˮֱ������ |
����ϡ����ʱ���а�ɫ������Ȼ���ɫ�����ܽ⣻�ٵ��백ˮʱ�а�ɫ���������Ҳ����ܽ⣬˵����ĩ�к���ZnO ����ϡ����ʱ���а�ɫ������Ȼ���ɫ�����ܽ⣻�ٵ��백ˮʱ�а�ɫ���������Ҳ����ܽ⣬˵����ĩ�к���ZnO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
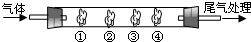
| B������� | �� | �� | �� | �� |
| ����ȡ�Լ� | ʯ����Һ | Ʒ����Һ | ���ۺ͵�ˮ���Һ | ������ |
| ���� | ��� ��� |
��ɫ ��ɫ |
��ɫ | dz��ɫ |
| ����SO2������ | ˮ��Һ������ | Ư���� | ��ԭ�� ��ԭ�� |
������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
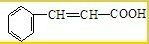
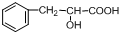 ��2009?����һģ���л���A��һ����Ҫ�����������м��壬��ṹ��ʽ���£�
��2009?����һģ���л���A��һ����Ҫ�����������м��壬��ṹ��ʽ���£�




�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�





�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com