
| A. | 比赛时,篮球内一般充填氮气 | B. | 比赛时,篮球内约有空气0.3mol | ||
| C. | 比赛时,篮球内约有空气14.8g | D. | 当25℃,170kPa时,Vm>24.5L/mol |
分析 A.篮球内一般填充空气;
B.压强与体积成反比,如果在170kPa时,空气的物质的量=$\frac{V}{{V}_{m}}$,100kPa时空气体积应该大于7.35L;
C.空气的平均摩尔质量为29g/mol,根据m=nM计算空气质量;
D.相同温度时,压强与气体摩尔体积成反比.
解答 解:A.篮球内一般填充空气,不需要填充氮气,故A错误;
B.压强与体积成反比,如果在170kPa时,空气的物质的量=$\frac{V}{{V}_{m}}$=$\frac{7.35L}{24.5L/mol}$=0.3mol,100kPa时空气体积应该大于7.35L,则空气物质的量应该大于0.3mol,故B错误;
C.内部空间体积大约是7.35L,比赛时内部压强约为170kPa,
如果压强是100kPa时,空气体积=$\frac{7.35L×170kPa}{100kPa}$=12.495L,
空气的平均摩尔质量为29g/mol,
则空气质量=$\frac{12.495L}{24.5L/mol}$×29g/mol=14.8g,故C正确;
D.相同温度时,压强与气体摩尔体积成反比,当25℃,170kPa时,Vm<24.5L/mol,故D错误;
故选C.
点评 本题考查物质的量有关计算,为高频考点,侧重考查学生分析判断能力,明确压强与气体体积关系是解本题关键,注意:气体摩尔体积受温度和压强影响,为易错题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol H2含有的分子数目为NA | |
| B. | 24g Mg变为Mg2+时失去的电子数目为NA | |
| C. | 1L 1mol•L-1CaCl2溶液中含有的Cl-离子数目为NA | |
| D. | 常温常压下,11.2LO2中含有的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| D. | 标准状况下,1molNa2O2的体积是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴有酚酞的碳酸氢钠溶液显红色,微热后红色加深,是因为碳酸氢钠分解生成了碳酸钠 | |
| B. | 用洁净的玻璃管向包有过氧化钠的脱脂棉吹气,脱脂棉燃烧,说明二氧化碳、水与过氧化钠的反应是放热反应 | |
| C. | 向溴水中滴入植物油,振荡后油层显无色,说明溴不溶于油脂 | |
| D. | 粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
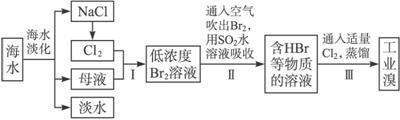
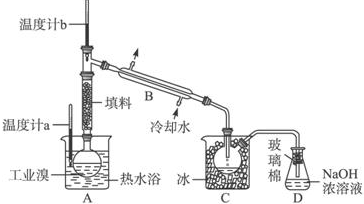
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com