
下列反应不属于氧化还原反应的是 ( )
A. 2H2O2 = 2H2O + O2↑; B.CuCl2+2NaOH==Cu(OH)2↓+2NaCl
C.2Na+2H2O=2NaOH+H2↑ D.3CO+Fe2O3 ==2Fe+3CO2
科目:高中化学 来源: 题型:
化学与生活密切相关。下列说法不正确的是
A.乙烯可作水果的催熟剂
 B.硅胶可作袋装食品的干燥剂
B.硅胶可作袋装食品的干燥剂
 C.福尔马林可作食品的保鲜剂
C.福尔马林可作食品的保鲜剂
D.氢氧化铝可作胃酸 的中和剂
的中和剂
查看答案和解析>>
科目:高中化学 来源: 题型:
.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确的是 ( )
A.该合金中铜与镁的物质的量之比是2 ︰1
B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C. NO2和N2O4 的混合气体中,NO2 的体 积分数是80%
积分数是80%
D. 得到2.54沉淀时,加入NaOH溶液的体积是600mL
查看答案和解析>>
科目:高中化学 来源: 题型:
相同体积的NaCl溶液(浓度为C1)和Na2SO4溶液(浓度为C2),若其中的Na+ 物质的量浓度相同,则它们的物质的量浓度C1和C2的关系是 ( )
A.C1 >C2 B.C1 =C2 C.C1 <C2 D.2 C1 =C2
查看答案和解析>>
科目:高中化学 来源: 题型:
在KClO3+6 H Cl(浓)=KCl+3Cl2↑+3H2O的反应中,氧化剂是___________,还原产物是_________,得电子与失电子个数比是____________,氧化产物与还原产物的质量比是________,试标出反应电子转移方向和数目_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
将浓度都为1mol/L的Na2CO3溶液和稀H2SO4按体积比2:1混合,则下列说法正确的是
A.混合溶液的pH<7
B.混合溶液中:c(SO42-)+c(OH-)< c(HCO3-)+c(H2CO3)+c(CO32-)
C.混合溶液中:c(Na+)+c(H+)<2[c(SO42-)+c(CO32-)]
D.混合溶液中离子浓度大小顺序是:c(Na+)>c(HCO3-)>c(OH-)>c(SO42-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,将Cl2通入KOH溶液中,反应得到KCl、KClO、KClO3的混合物,经测定c(ClO—): c(ClO3—)=1:3,则此反应中被还原氯元素与被氧化氯元素的质量比为( )
A.21:5 B.11:3 C.3:1 D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知某反应的平衡常数表达式为:K=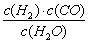 ,则它所对应反应的化学方程式是 ▲ 。
,则它所对应反应的化学方程式是 ▲ 。
(2) 合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
CH3OH(g) △H=-90.8 kJ·mol-1,t℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应l0min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度(mol/L) | 0.2 | 0.1 | 0.4 |
(A)该时间段内反应速率v(H2)= ▲
(B)比较此时正、逆反应速率的大小:v正 ▲ v逆(填“>”、“<”或“=”)
(C)反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡向 ▲
(填“逆向”、“正向”或“不”)移动,平衡常数K ▲ (填“增大”、“减小” 或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com