
| A. | H2、D2互为同位素 | B. | 碘晶体、碘蒸气是同素异形体 | ||
| C. | NH4OCN、CO(NH2)2互为同分异构体 | D. | C2H4与C3H6一定是同系物 |
分析 A.质子数相同中子数不同的同一元素的原子互称同位素;
B.由同种元素组成的不同单质叫同素异形体;
C.分子式相同结构不同的化合物属于同分异构体;
D.同系物:结构相似,在分子组成上相差一个或若干个CH2原子团的有机化合物.
解答 解:A.H2、D2是单质,不是原子,不为同位素,故A错误;
B.碘晶体、碘蒸气是碘单质的不同状态,故B错误;
C.氰酸铵(NH4OCN)与尿素[CO(NH2)2]的分子式相同但结构不同,所以属于同分异构体,故C正确;
D.C3H6可能为环烷烃,乙烯一定是烯烃,结构不一定相似,故D错误.
故选C.
点评 本题考查了同位素、同素异形体、同分异构体、同系物等概念,难度不大,注意这几个概念的区别.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 凡需加热的反应一定是吸热反应 | |
| B. | 只有分解反应才是吸热反应 | |
| C. | 吸热反应一定不能在常温下进行 | |
| D. | 已知CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的同系物分子中,碳原子数比苯多 | |
| B. | 苯环受侧链影响,易被氧化 | |
| C. | 侧链受苯环影响,易被氧化 | |
| D. | 分子中含有碳碳双键的缘故 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1的Na2CO3溶液中离子浓度关系:c (Na+)+c (H+)=c (CO32-)+c (HCO3-)+c (H2CO3) | |
| B. | 0.1 mol•L-1的NH4Cl和0.1 mol•L-1的NH3•H2O等体积混合后溶液中的离子浓度关系:c (Cl-)>c (NH4+)>c (H+)>c (OH-) | |
| C. | 常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子浓度关系:c (Na+)=c (CH3COO-) | |
| D. | 0.1 mol•L-1的NaHCO3溶液中离子浓度关系:c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3Cl只有一种 | B. | CH2Cl2只有一种 | C. | CHCl3只有一种 | D. | CCl4只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 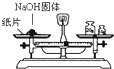 用托盘天平快速称量一定质量的氢氧化钠固体 | |
| B. |  使用橡皮管能使漏斗中的水顺利流下 | |
| C. |  分离Cl2与KI溶液反应生成的碘 | |
| D. |  分离Cl2与KI溶液反应生成的碘 | |
| E. |  比较Na2CO3和NaHCO3的热稳定性 | |
| F. |  用焰色反应检验钾离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同| A. | ①②⑤ | B. | ③④⑦ | C. | ①④⑥ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com