
ЁОЬтФПЁПТЬЗЏжаFeSO4ЁЄ7H2OКЌСПЕФВтЖЈЃЌШєгУШнСПЗЈВтЖЈТЬЗЏжаFeSO4ЁЄ7H2OЕФКЌСПЁЃЕЮЖЈЗДгІЪЧЃК5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2OЁЃ
ЪЕбщЗНАИШчЯТЃКЂйГЦШЁ15.041gТЬЗЏВњЦЗЃЌШмНтЃЌдк250mLШнСПЦПжаЖЈШнЁЃ
ЂкСПШЁ25.00mL Д§ВтШмвКгкзЖаЮЦПжаЁЃ
ЂлгУ0.0500mol/LKMnO4ШмвКЃЈСђЫсЫсЛЏЃЉЕЮЖЈжСжеЕуЃЌМЧТМГѕЖСЪ§КЭФЉЖСЪ§ЁЃ
Ђм ЁЃ
Ђн Ъ§ОнДІРэЁЃ
ЃЈ1ЃЉЩЯЪіЪЕбщЗНАИжаЕФВНжшЂмЪЧ______ЁЃНрОЛЕФЕЮЖЈЙмдкЕЮЖЈЧАБиаыНјааЕФВйзїгаЃК
ЂйМьбщЛюШћЪЧЗёТЉЫЎЃЛ
Ђк_______ЃЛ
ЂлЯђЕЮЖЈЙмжаМгШыKMnO4БъзМШмвКЕН0ПЬЖШвдЩЯЃЌИЯзпМтзьВПЮЛЕФЦјХнЃЌЕїНкГѕЖСЪ§ЁЃ
ЃЈЪ§ОнДІРэЃЉФГаЁзщЭЌбЇЕФЪЕбщЪ§ОнМЧТМШчЯТЃК
ЪЕбщДЮЪ§ | ГѕЖСЪ§ЃЈmLЃЉ | ФЉЖСЪ§ЃЈmLЃЉ |
1 | 0.20 | 21.40 |
2 | 0.00 | 21.00 |
3 | 1.60 | 26.60 |
ЃЈ2ЃЉЩЯЪібљЦЗжаFeSO4ЁЄ7H2OЕФжЪСПЗжЪ§ЮЊ_______ЃЈгУаЁЪ§БэЪОЃЌБЃСєШ§ЮЛаЁЪ§ЃЉЁЃ
ЁОД№АИЁПжиИДВйзїЂкЂл1ЁЋ2ДЮ гУеєСѓЫЎЯДЕг2ЁЋ3ДЮЃЌдйгУИпУЬЫсМиБъзМШмвКШѓЯДЕЮЖЈЙм2ЁЋ3ДЮ 0.975
ЁОНтЮіЁП
ЃЈ1ЃЉЮЊМѕЩйЪЕбщЮѓВюЃЌПЩжиИДЂкЂл12ДЮЃЌЛђзіЦНааЪЕбщ12ДЮЃЛНрОЛЕФЕЮЖЈЙмдкЕЮЖЈЧАБиаыНјааМьТЉКЭШѓЯДЃЌПЩгУеєСѓЫЎЯДЕг23ДЮЃЌдйгУИпУЬЫсМиБъзМШмвКШѓЯДЕЮЖЈЙм23ДЮЃЌ
ЙЪД№АИЮЊЃКжиИДВйзїЂкЂл12ДЮЃЛгУеєСѓЫЎЯДЕг23ДЮЃЌдйгУИпУЬЫсМиБъзМШмвКШѓЯДЕЮЖЈЙм23ДЮЃЛ
ЃЈ2ЃЉгУСђЫсЫсЛЏЕФ0.01000mol/LKMnO4ШмвКЕЮЖЈжСжеЕуЃЌЯћКФKMnO4ШмвКЬхЛ§ЕФЪ§ОнжаЕкШ§зщЪ§ОнЮѓВюНЯДѓЃЌЩсШЅЃЌвђДЫKMnO4ШмвКЬхЛ§ЕФЦНОљжЕЮЊ![]() =20.10mLЃЌдђ:
=20.10mLЃЌдђ:
5Fe2++MnO4+8H+ЈT5Fe3++Mn2++4H2O
51
n(Fe2+) 0.05000mol/LЁС0.0210L
МЦЫуЕУЕНЃКn(Fe2+)=0.05000mol/LЁС0.0210LЁС5 =0.00525 molЃЛ
дђ250mLШмвКжаКЌFe2+=0.00525 molЁС![]() =0.0525 molЃЛ
=0.0525 molЃЛ
FeSO47H2OЮяжЪЕФСПЮЊ0.0525molЃЌжЪСП=0.0525 molЁС278g/mol=14.595 gЃЛ
жЪСПЗжЪ§=![]() ЁС100%=97.5%=0.975ЃЌ
ЁС100%=97.5%=0.975ЃЌ
ЙЪД№АИЮЊЃК0.975ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПX(g)+3Y(g) ![]() 2Z(g) ІЄH=Ѓa kJЁЄmolЁЅ1 ЃЌвЛЖЈЬѕМўЯТЃЌНЋ1 mol XКЭ3 mol YЭЈШы2LЕФКуШнУмБеШнЦїжаЃЌЗДгІ10minЃЌВтЕУYЕФЮяжЪЕФСПЮЊ2.4 molЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
2Z(g) ІЄH=Ѓa kJЁЄmolЁЅ1 ЃЌвЛЖЈЬѕМўЯТЃЌНЋ1 mol XКЭ3 mol YЭЈШы2LЕФКуШнУмБеШнЦїжаЃЌЗДгІ10minЃЌВтЕУYЕФЮяжЪЕФСПЮЊ2.4 molЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
A.10minФкЃЌЯћКФ0.2 mol XЃЌЩњГЩ0.4 mol Z
B.Ек10minЪБЃЌXЕФЗДгІЫйТЪЮЊ0.01 molЁЄLЁЅ1ЁЄminЁЅ1
C.10minФкЃЌYЕФЦНОљЗДгІЫйТЪЮЊ0.03 molЁЄLЁЅ1ЁЄsЁЅ1
D.10minФкЃЌXКЭYЗДгІЗХГіЕФШШСПЮЊa kJ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРћгУЫЎюмПѓЃЈжївЊГЩЗжЮЊCo2O3ЃЌКЌЩйСПFe2O3ЁЂAl2O3ЁЂMnOЁЂMgOЁЂCaOЁЂSiO2ЕШЃЉПЩвджЦШЁЖржжЛЏЙЄЪдМСЃЌвдЯТЮЊВнЫсюмОЇЬхКЭТШЛЏюмОЇЬхЕФжЦБИСїГЬЃЌЛиД№ЯТСаЮЪЬтЃК
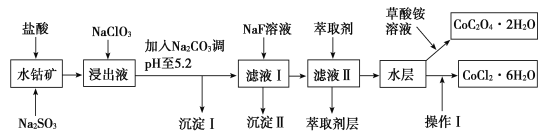
вбжЊЃКЂйНўГівКжаКЌгаЕФбєРызгжївЊгаH+ЁЂCo2+ЁЂFe2+ЁЂMn2+ЁЂAl3+ЁЂMg2+ЁЂCa2+ЕШЁЃ
ЂкГСЕэЂёжажЛКЌгаСНжжГСЕэЁЃ
ЂлСїГЬжаВПЗжбєРызгвдЧтбѕЛЏЮяаЮЪНГСЕэЪБШмвКЕФpHМћБэЃК
ГСЕэЮя | ПЊЪМГСЕэ | ЭъШЋГСЕэ |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Co(OH)2 | 7.6 | 9.2 |
Al(OH)3 | 4.0 | 5.2 |
Mn(OH)2 | 7.7 | 9.8 |
ЃЈ1ЃЉНўГіЙ§ГЬжабѕЛЏМСгыЛЙдМСЮяжЪЕФСПжЎБШЮЊ___ЁЃ
ЃЈ2ЃЉNaClO3дкНўГівКжаЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ___ЁЃ
ЃЈ3ЃЉМгШыNa2CO3ЕїpHжС5.2ЃЌФПЕФЪЧ___ЃЛнЭШЁМСВуКЌУЬдЊЫиЃЌдђГСЕэЂђЕФжївЊГЩЗжЮЊ__ЁЃ
ЃЈ4ЃЉВйзїЂёАќРЈЃКНЋЫЎВуМгШыХЈбЮЫсЕїећpHЮЊ2ЁЋ3ЃЌ___ЁЂ___ЁЂЙ§ТЫЁЂЯДЕгЁЂМѕбЙКцИЩЕШЙ§ГЬЁЃ
ЃЈ5ЃЉЮЊВтЖЈДжВњЦЗжаCoCl2ЁЄ6H2OЕФКЌСПЃЌГЦШЁвЛЖЈжЪСПЕФДжВњЦЗШмгкЫЎЃЌМгШызуСПЯѕЫсЫсЛЏЕФЯѕЫсвјШмвКЃЌЙ§ТЫЁЂЯДЕгЁЂИЩдяЃЌВтГСЕэжЪСПЁЃЭЈЙ§МЦЫуЗЂЯжДжВњЦЗжаCoCl2ЁЄ6H2OжЪСПЗжЪ§Дѓгк100%ЃЌЦфдвђПЩФмЪЧ___ЃЈЛиД№вЛЬѕдвђМДПЩЃЉЁЃ
ЃЈ6ЃЉНЋ5.49gВнЫсюмОЇЬх(CoC2O4ЁЄ2H2O)жУгкПеЦјжаМгШШЃЌЪмШШЙ§ГЬжаВЛЭЌЮТЖШЗЖЮЇФкЗжБ№ЕУЕНвЛжжЙЬЬхЮяжЪЃЌЦфжЪСПШчБэЁЃ
ЮТЖШЗЖЮЇ/Ёц | 150ЁЋ210 | 290ЁЋ320 |
ЙЬЬхжЪСП/g | 4.41 | 2.41 |
ОВтЖЈЃЌећИіЪмШШЙ§ГЬЃЌжЛВњЩњЫЎеєЦјКЭCO2ЦјЬхЃЌдђ290ЁЋ320ЁцЮТЖШЗЖЮЇЃЌЪЃгрЕФЙЬЬхЮяжЪЛЏбЇЪНЮЊ___ЁЃ[вбжЊЃКCoC2O4ЁЄ2H2OЕФФІЖћжЪСПЮЊ183gЁЄmol-1]
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУCl2КЭCa(OH)2жЦБИЩйСПЦЏЗлОЋЃЈвЛжжКЌТШЯћЖОМСЃЉЕФзАжУШчЯТЁЃ
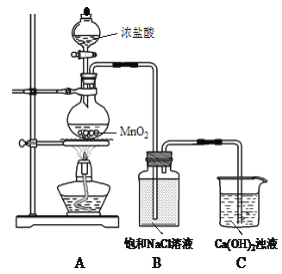
ЃЈ1ЃЉAЮЊТШЦјЗЂЩњзАжУЁЃAжаЗДгІЗНГЬЪНЪЧ________ЁЃ
ЃЈ2ЃЉBЕФзїгУЪЧЮќЪеЛгЗЂГіЕФHClЁЃHClПЩФмЖджЦБИЦЏЗлОЋдьГЩЕФгАЯьЪЧ________ЁЃ
ЃЈ3ЃЉгУCl2КЭCa(OH)2жЦБИЕФЦЏЗлОЋЃЌЦфгааЇГЩЗжЪЧ_________ЁЃ
ЃЈ4ЃЉЦЏЗлОЋГЃгУгкгЮгОГиЕФЯћЖОЃЌЦ№ЯћЖОзїгУЕФЪЧHClOЁЃЦЏЗлОЋдкЫЎжаЪЭЗХHClOЕФЭООЖШчЯТЃК
ЭООЖвЛЃКCa(ClO)2 + 2H2O Ca(OH)2 + 2HClO
ЭООЖЖўЃКCa(ClO)2 + H2O + CO2 ЃН________+ _______ЃЈАбЗДгІВЙГфЭъећЃЉ
ЃЈ5ЃЉГиЫЎЕФЫсМюадЖдЦЏЗлОЋЕФЯћЖОаЇЙћгАЯьУїЯдЁЃ
ЂйГиЫЎМюадЙ§ЧПЃЌЩБЖОзїгУЛс________ЃЈЬюЁАдіЧПЁБЛђЁАМѕШѕЁБЃЉЁЃ
ЂкГиЫЎЫсадЙ§ЧПЃЌЛсДЬМЄблОІКЭЦЄЗєЁЃЭЈГЃМгШыNa2CO3ЁЂNaHCO3вдНЕЕЭЫсадЃЌЦ№ЕННЕЕЭЫсадзїгУЕФРызгЗжБ№ЪЧ________ЃЈЬюРызгЗћКХЃЉЁЃ
ЃЈ6ЃЉФГНьАТдЫЛсЦкМфЃЌЗЂЩњСЫЪвЭтгЮгОГиЫЎБфТЬЕФЪТМўЃЌГЩЮЊЕБЪБЕФвЛДѓаТЮХЁЃгаЙиИК
д№ШЫЫЕЃЌГиЫЎБфТЬЪЧдхРрЩњГЄдьГЩЕФЁЃИУгЮгОГиУПИєвЛЖЮЪБМфОЭвЊЭЖЗХКЌТШЯћЖОМСЃЌЕБдйДЮЭЖЗХЪБЃЌЮѓЭЖСЫЙ§бѕЛЏЧтЃЈH2O2ЃЉЯћЖОМСЁЃЯћЖОМСЮЊЪВУДВЛЦ№зїгУСЫЃП_______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШЫРрЩњЛюРыВЛПЊЛЏбЇЃЌвдЯТЪЧВЙЬњМСКЭЮИвЉЕФСНеХБъЧЉЕФВПЗжаХЯЂЁЃ
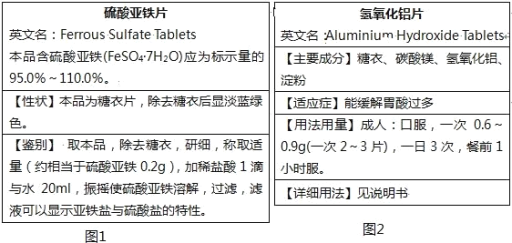
ЃЈ1ЃЉИљОнЁАСђЫсбЧЬњЦЌЁББъЧЉШчЭМ1ЛиД№ЃК
ЂйСђЫсбЧЬњЦЌжаЃЌЬЧвТЕФзїгУЪЧ_______ЃЛ
ЂкМьбщСђЫсбЧЬњЪЧЗёБЛбѕЛЏЕФЪдМСЪЧ_______ЃЛ
ЂлСђЫсбЮЕФМјБ№ЗДгІЕФРызгЗНГЬЪНЪЧ______ЃЛ
ЂмМјБ№жаЃЌЁАМгЯЁбЮЫс1ЕЮЁБЕФзїгУЪЧ_______ЃЈбЁЬюађКХЃЉЃЛ
A.ЗРжЙбЧЬњРызгБЛбѕЛЏ B.вжжЦбЧЬњРызгЫЎНт
ЃЈ2ЃЉИљОнЧтбѕЛЏТСЦЌБъЧЉШчЭМ2ЛиД№ЃК
ЂйФмЛКНтЮИЫсЙ§ЖрЕФгааЇГЩЗжЪЧ______ЃЛ
ЂкаДГіЧтбѕЛЏТСжаКЭЮИЫсЗДгІЕФРызгЗНГЬЪН_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАБЕФДпЛЏбѕЛЏЪЧжЦЯѕЫсЕФжївЊЗДгІжЎвЛ,ЦфЮЂЙлЪОвтЭМШчЯТЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ

A.МзЕФЛЏбЇЪНЮЊNH3 , ЦфЫЎШмвКГЪМюадB.ИУЗДгІжадЊЫиЕФЛЏКЯМлЖМЗЂЩњИФБф
C.ИУЗДгІжаМзЁЂввЕФжЪСПБШЮЊ17 :32D.ЩњГЩЮяБћЁЂЖЁЕФЗжзгИіЪ§БШЮЊ1:2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊAЮЊе§бЮЁЃИљОнЯТСаБфЛЏНјааЭЦЖЯЃЌЛиД№гаЙиЮЪЬтЃК

ЃЈ1ЃЉЭЦЖЯAЁЂBЁЂCЁЂDЕФЛЏбЇЪНЃКA________ЁЂB________ЁЂC________ЁЂD________ЁЃ
ЃЈ2ЃЉаДГіЯТСаЗДгІЕФРызгЗНГЬЪНЃК
ЗДгІЂйЩњГЩЦјЬхBЃК__________________________________________________ЃЛ
ЗДгІЂкАзЩЋГСЕэШмНтЃК________________________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкЫФИіВЛЭЌЕФШнЦїжаЃЌдкВЛЭЌЕФЬѕМўЯТНјааКЯГЩАБЕФЗДгІЃЌИљОнЯТСадкЯрЭЌЪБМфФкВтЖЈЕФНсЙћХаЖЯЃЌЛЏбЇЗДгІЫйТЪзюПьЕФЪЧ ЃЈ ЃЉ
A.v(H2)=0.2 molЁЄL-1ЁЄmin-1B.v(H2)=0.04 molЁЄL-1ЁЄs-1
C.v(N2)=0.01 molЁЄL-1ЁЄs-1D.v(N2)=0.2 molЁЄL-1ЁЄmin-1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЬхЛ§2LЕФУмБеШнЦїжаМгШыЗДгІЮяN2ЁЂH2ЃЌЗЂЩњШчЯТЗДгІЃКN2(g)ЃЋ3H2(g)![]() 2NH3(g)ЁЃЗДгІЙ§ГЬжаЕФВПЗжЪ§ОнШчЯТБэЫљЪОЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
2NH3(g)ЁЃЗДгІЙ§ГЬжаЕФВПЗжЪ§ОнШчЯТБэЫљЪОЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЮяжЪЕФСП/ mol ЪБМф/min | n(N2) | n(H2) | n(NH3) |
0 | 1.0 | 1.2 | 0 |
2 | 0.9 | ||
4 | 0.75 | ||
6 | 0.3 |
A. 0ЁЋ2 minФкЃЌNH3ЕФЗДгІЫйТЪЮЊ0.1 molЁЄLЁЅ1ЁЄminЁЅ1
B. 2 minЪБЃЌ H2ЕФЮяжЪЕФСП0.3 mol
C. 4 minЪБЃЌЗДгІвбДяЕНЦНКтзДЬЌЃЌДЫЪБе§ЁЂФцЗДгІЕФЫйТЪЖМЮЊ0
D. 4ЁЋ6 minФкЃЌШнЦїФкЦјЬхЗжзгЕФзмЮяжЪЕФСПВЛБф
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com