
自来水常用Cl2消毒。某学生用这种自来水配制下列物质的溶液,不会产生明显的药品变质问题的是( )
| A.AgNO3 | B.NaCl | C.FeCl2 | D.Na2SO3 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
下列关于氯水的叙述正确的是
| A.新制氯水中只含Cl2和H2O分子 | B.光照氯水有气泡放出,该气体是Cl2 |
| C.氯水放置一段时间后颜色将变深 | D.新制氯水可使紫色石蕊试液先变红后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
漂白粉在空气中放置易失效的主要原因是( )
| A.Ca(ClO)2不稳定,易分解 | B.Ca(ClO)2易吸收水分而潮解 |
| C.Ca(ClO)2跟空气中的水和CO2反应 | D.Ca(ClO)2跟空气中的CO2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硫酸是用途广泛的化工原料,可作脱水荆、吸水荆、氧化剂和催化荆等。
工业制硫酸铜的方法很多。
(1)方法一、用浓硫酸制取硫酸铜。该反应的化学方程式是____ ,
此法的最大缺点是__ __。
(2) 方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示: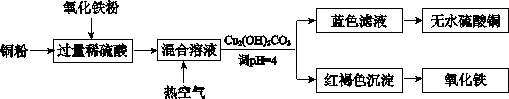
稀硫酸、铜和氧化铁反应的离子方程式是 、 ;向混合溶液中通人热空气的反应的离子方程式是 ;由滤液得到无水硫酸铜的实验操作是 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知某物质X能发生如下转化: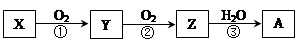
下列有关上述转化关系中物质及其反应的叙述错误的是
| A.若X为N2或NH3,则A为硝酸 |
| B.若X为S或H2S,则A为硫酸 |
| C.若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y |
| D.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
14gCu、Ag合金与足量某浓度的硝酸反应,将放出的气体与1.12L O2(标况)混合,恰好能被水全部吸收生成硝酸,则合金中Cu的质量为
| A.1.6g | B.3.2g | C.6.4g | D.9.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列现象或事实能用同一原理解释的是
| A.浓硫酸、浓盐酸暴露在空气中浓度降低 |
| B.氯水、活性炭使红墨水褪色 |
| C.苯、四氯化碳加入溴水中,振荡、静置,水层颜色变浅 |
| D.漂白粉、亚硫酸钠长期暴露在空气中变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氯气是一种重要的工业原料。工业上利用反应在3Cl2+8NH3=N2+6NH4Cl检查氯气管道是否漏气。下列说法正确的是
| A.若管道漏气遇氨就会产生白雾 | B.该反应利用了氨气的还原性 |
| C.该反应属于复分解反应 | D.生成6molNH4Cl有18mol电子转移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com