
工业上用铝土矿 (主要成分为Al2O3、Fe2O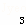 、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下:
、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下: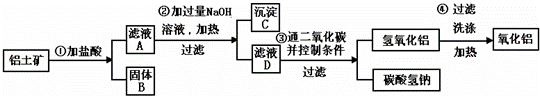
(1)第一步在铝土矿中加入盐酸后的实验基本操作是 ,若在固体B中加入氢氧化钠溶液 会 (填”会”或”不会”)发生反应,若会,则写出反应的离子方程式 S
(2)验证滤液A中是否含Fe3+,可取少量滤液A并加入 (填试剂化学式),现象是 .
(3)在整个操作过程中 (填“是”“否”)有氧化还原反应;写出碳酸氢钠的一种用 .
考点:
物质分离和提纯的方法和基本操作综合应用.
分析:
由流程可知,加盐酸,只有SiO2不反应,氧化铝、氧化铁均与盐酸反应,过滤沉淀为SiO2;滤液中加过量NaOH,铝离子转化为偏铝酸钠,铁离子转化沉淀,过滤后,滤液D与二氧化碳反应生成氢氧化铝和碳酸氢钠,最后氢氧化铝分解生成氧化铝,以此来解答.
解答:
解:(1)①加盐酸,只有SiO2不反应,氧化铝、氧化铁均与盐酸反应,所以加入盐酸后的实验基本操作是过滤,二氧化硅是酸性氧化物,能与碱反应生成硅酸钠,SiO2+2OH﹣=SiO32﹣+H2O,故答案为:过滤;会;SiO2+2OH﹣=SiO32﹣+H2O;
(2)Fe3+与硫氰化钾溶液反应,使溶液变红色,检验滤液A中是否含Fe3+离子的方法为:取少量滤液A,向其中加入硫氰化钾溶液,溶液变红色,说明滤液中含Fe3+,溶液不变红色,说明滤液中不含Fe3+,
故答案为:硫氰化钾;取少量滤液A,向其中加入硫氰化钾溶液,溶液变红色,说明滤液中含Fe3+,溶液不变红色,说明滤液中不含Fe3+;
(3)整个过程所有反应无化合价的变化,无氧化还原反应;碳酸氢钠可用于制纯碱或做发酵粉等,
故答案为:否;制纯碱或做发酵粉等.
点评:
本题以氧化铝提取工艺流程为载体考查混合物分离实验方案的设计,为高频考点,涉及无机物推断、元素化合物性质及相互转化、除杂的方法、离子方程式等,侧重分析与实验能力的考查,题目难度中等.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
根据气象台报道,近年每到春季,沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞.雾属于下列分散系中的( )
|
| A. | 溶液 | B. | 悬浊液 | C. | 乳浊液 | D. | 胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列信息写出符合要求的有机物的结构简式.
(1)若某有机物的分子量为128,若该有机物为链烃,则分子式为 ,若该烃一氯代物只有二种,则该烃的结构简式为 或 ,若该有机物为烃的含氧衍生物,且是饱和一元的有机物,则其分子式为
(2)某有机物仅由C、H、O三种元素组成,且C、H、O原子个数之比为1:2:1,若该有机物为醛类,则其结构简式为: ,若该有机物为糖类,则其结构简式为 ,若该有机物分子式为C3H6O3,且两分子该有机物可形成六元环状酯,则C3H6O3结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 非金属元素的原子最外层电子数都大于或等于4 |
|
| B. | 只有非金属能形成含氧酸或含氧酸盐 |
|
| C. | Na2O2中阴阳离子的个数比为1:1 |
|
| D. | 非金属元素组成的化合物不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列针对甲、乙、丙、丁四种实验及装置的说法,不合理的是( )
|
| A. |
可用来证明碳的非金属性比硅强 |
|
| B. |
装置可用于碘水中碘的萃取及分液 |
|
| C. |
用如图示的方法检查此装置的气密性 |
|
| D. |
装置:从①进气可收集NO;从②进气可收集NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.丙烯分子中有8个 σ 键,1个 π 键
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.NCl3和BCl3分子中,中心原子都采用sp3杂化
D.在“冰→水→水蒸气→氧气和氢气”的变化过程中,各阶段被破坏的粒子间主要的相互作用依次是氢键、分子间作用力、极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
为了减少大气污染,许多城市推广汽车使用清洁燃料.目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG).这两类燃料的主要成份都是( )
|
| A. | 碳水化合物 | B. | 碳氢化合物 | C. | 氢气 | D. | 醇类 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验:
①0.1mol•L﹣1AgNO3溶液和0.1mol•L﹣1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1mol•L﹣1KI溶液,出现浑浊;
③向沉淀c中滴加0.1mol•L﹣1KI溶液,沉淀变为黄色.
下列分析不正确的是( )
|
| A. | 浊液a中存在沉淀溶解平衡:AgCl(s)⇌Ag+(aq)+Cl﹣(aq) |
|
| B. | 滤液b中不含有Ag+ |
|
| C. | ③中颜色变化说明AgCl转化为AgI |
|
| D. | 实验可以证明AgI比AgCl更难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知aAn+、bB(n+1)+、cCn﹣、dD(n+1)﹣具有相同的电子层结构,关于A、B、C、D四种元素叙述正确的是( )
A. 气态氢化物的稳定性:D>C B. 原子序数:b>a>c>d
C. 离子的还原性:cCn﹣>dD(n+1)﹣ D. 离子的氧化性:aAn+>bB(n+1)+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com