
| 选项 | A | B | C | D |
| 实验方案 | 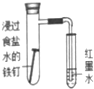 | 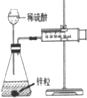 | 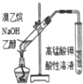 | 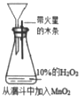 |
| 现象 | 导管中有红色柱 | 注射器的活塞往外推 | 高锰酸钾酸性溶液褪色 | 带火星的木条复燃 |
| 结论或作用 | 证明铁钉发生吸氧腐蚀 | 可用于测定反应物浓度对反应速率的影响 | 溴乙烷与NaOH乙醇溶液反应生成的气体是乙烯 | MnO2可与H2O2反应生成O2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.中性条件下,钢铁发生吸氧腐蚀,导致导气管中水液面上升;
B.应该用分液漏斗;
C.乙醇也能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色;
D.二氧化锰作催化剂.
解答 解:A.中性条件下,钢铁发生吸氧腐蚀,导致导气管中水液面上升,所以可以实现实验目的,故A选;
B.应该用分液漏斗,否则生成的氢气逸出,故B不选;
C.乙醇也能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,应该用溴水检验乙烯,故C不选;
D.二氧化锰作催化剂,能加快反应速率,故D不选;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及金属腐蚀与防护、反应速率测定、物质检验等知识点,明确实验原理及物质性质、实验基本操作规范性是解本题关键,易错选项是C,注意物质检验时要排除其它因素的干扰.


科目:高中化学 来源: 题型:选择题
| A. | 2mol/L盐酸与锌反应时,加入4mol/L的氯化钠溶液,生成氢气的速率加快 | |
| B. | 对于可逆反应2CO+2NO?N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 | |
| C. | 工业上合成氨是放热反应,升高温度,正反应速率减慢 | |
| D. | 在K2SO4和BaCl2两溶液反应时,增大压强,生成沉淀速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
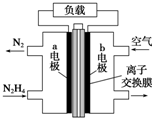
| A. | 放电时,电流从b极经过负载流向a极 | |
| B. | b极发生氧化反应 | |
| C. | a极的反应式为N2H4+4OH--4e-=N2+4H2O | |
| D. | 电池中的离子交换膜需选用阳离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
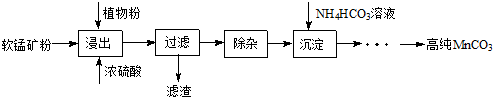
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe3+是人体所需微量元素 | B. | 苯酚不能用于杀菌消毒 | ||
| C. | 氢气是未来的一种理想燃料 | D. | 乙醇是不可再生的生物质能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧原子的原子结构示意图: | |
| B. | 羟基的结构式:O-H | |
| C. | 用电子式表示Na2O的形成过程: | |
| D. | 组成为C2H6O的分子中可能只存在极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 +12MnO${\;}_{4}^{-}$+36H+→
+12MnO${\;}_{4}^{-}$+36H+→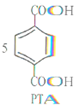 +12Mn2++28H2O.
+12Mn2++28H2O.| A. | PTA是该反应的氧化产物 | B. | 消耗1molPX,共转移8mol电子 | ||
| C. | PX含苯环的同分异构体还有3种 | D. | PTA与乙二醇可以发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性酸:HNO3、H3PO4、HClO4 | |
| B. | 干燥剂:碱石灰、硅胶、无水氯化钙 | |
| C. | 酸性氧化物:SiO2、Cl2O、CrO3 | |
| D. | 危险化学品:天然气、金属钠、氯酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
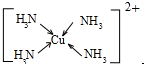 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com