
| A£® | ”÷H2£¾”÷H3£¾”÷H1 | B£® | ”÷H3£¾”÷H2£¾”÷H1 | C£® | ”÷H3£¾”÷H1£¾”÷H2 | D£® | ”÷H1£¾”÷H2£¾”÷H3 |
·ÖĪö ÓÉøĒĖ¹¶ØĀÉæÉÖŖ£¬¢Ū”Į2-¢Ś”Į2=a£¬¢Ū”Į2-¢Ł”Į2=b£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗÓÉŅŃÖŖ·“Ó¦¼°øĒĖ¹¶ØĀÉæÉÖŖ£¬¢Ū”Į2-¢Ś”Į2=a£¬¢Ū”Į2-¢Ł”Į2=b£¬
Ōņ2”÷H3-2”÷H2£¼0£¬¼“”÷H2£¾”÷H3£»
2”÷H3-2”÷H1£¾0£¬¼“”÷H3£¾”÷H1£¬
×ŪŗĻĖłŹö£¬”÷H1”¢”÷H2”¢”÷H3Óɓ󵽊”µÄĖ³ŠņŹĒ”÷H2£¾”÷H3£¾”÷H1£¬
¹ŹŃ”A£®
µćĘĄ ±¾Ģā漲鷓ӦČČÓėģŹ±ä£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŅŃÖŖ·“Ó¦ÓėÄæ±ź·“Ó¦µÄ¹ŲĻµ”¢øĒĖ¹¶ØĀɵÄÓ¦ÓĆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāøĒĖ¹¶ØĀɼ°ģŹ±äµÄ±Č½Ļ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | Äæ µÄ | ·ÖĄė·½·Ø | Ō Ąķ |
| A | ·ÖĄėČÜÓŚĖ®ÖŠµÄµā | ŅŅ“¼ŻĶČ” | µāŌŚŅŅ“¼ÖŠµÄČܽā¶Č½Ļ“ó |
| B | ·ÖĄėŅŅĖįŅŅõ„ŗĶŅŅ“¼ | ·ÖŅŗ | ŅŅĖįŅŅõ„ŗĶŅŅ“¼µÄĆÜ¶Č²»Ķ¬ |
| C | ³żČ„ŅŅĶéÖŠ»ģÓŠµÄŅŅĻ© | ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĻ“Ęų | ŅŅĻ©ÓėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ·“Ó¦¶ųŅŅĶé²»ÄÜ |
| D | ³żČ„ŅŅĖįŅŅõ„ÖŠ»ģÓŠµÄŅŅĖį | ÓƱ„ŗĶĢ¼ĖįÄĘČÜŅŗĻ“µÓŗó·ÖŅŗ | ŅŅĖįÄÜÓėĢ¼ĖįÄĘ·“Ӧɜ³ÉČÜÓŚĖ®µÄŃĪ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
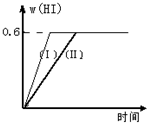 ¢ņ½«1mol I2£Øg£©ŗĶ2mol H2ÖĆÓŚ2LĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗI2£Øg£©+H2£Øg£©?2HI£Øg£©£»”÷H£¼0£¬²¢“ļĘ½ŗā£®HIµÄĢå»ż·ÖŹżw£ØHI£©Ėꏱ¼ä±ä»ÆČēĶ¼ĒśĻߣآņ£©ĖłŹ¾£ŗ
¢ņ½«1mol I2£Øg£©ŗĶ2mol H2ÖĆÓŚ2LĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗI2£Øg£©+H2£Øg£©?2HI£Øg£©£»”÷H£¼0£¬²¢“ļĘ½ŗā£®HIµÄĢå»ż·ÖŹżw£ØHI£©Ėꏱ¼ä±ä»ÆČēĶ¼ĒśĻߣآņ£©ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆøߊ§“߻ƼĮ£¬æÉŹ¹CO2µÄĘ½ŗā×Ŗ»ÆĀŹŌö“ó | |
| B£® | µ„Ī»Ź±¼äÄŚĻūŗÄCO2ŗĶH2µÄĪļÖŹµÄĮæ±ČĪŖ1£ŗ3Ź±£¬·“Ó¦“ļµ½Ę½ŗā | |
| C£® | ¼°Ź±·ÖĄė³öCH3OHŗĶH2OæÉĢįøßCO2ŗĶH2µÄ×Ŗ»ÆĀŹ | |
| D£® | ÉżøßĪĀ¶ČæÉŹ¹øĆ·“Ó¦ĻņÕż·“Ó¦·½ĻņŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Ņ»¶ØĪĀ¶ČĻĀ£¬·“Ó¦MgCl2£Øl£©=Mg£Øl£©+Cl2£Øg£©µÄ”÷H£¾0”¢”÷S£¾0 | |
| B£® | Ė®½ā·“Ó¦NH4++H2O?NH3•H2O+H+“ļµ½Ę½ŗāŗó£¬ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ | |
| C£® | AlCl3ČÜŅŗÕōøÉ”¢×ĘÉÕÖĮŗćÖŲ£¬×īÖÕŹ£Óą¹ĢĢåŹĒAlCl3 | |
| D£® | ¶ŌÓŚ·“Ó¦2H2O2=2H2O+O2”ü£¬¼ÓČėMnO2»ņÉżøßĪĀ¶Č¶¼ÄܼÓæģO2µÄÉś³ÉĖŁĀŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ijČÜŅŗ$\stackrel{AgNO_{3}}{”ś}$Éś³É°×É«³Įµķ£¬ŌņŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠCl- | |
| B£® | ijČÜŅŗ$\stackrel{BaCl_{2}}{”ś}$Éś³É°×É«³Įµķ£¬ŌņŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠSO42- | |
| C£® | ijČÜŅŗ$\stackrel{Na_{2}CO_{3}}{”ś}$ÓŠĘųĢå²śÉś£¬ŌņŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠH+ | |
| D£® | ijČÜŅŗ$\stackrel{Ļ”HCl}{”ś}$ÓŠĘųĢå²śÉś£¬ŌņŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠCO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com