
【题目】苯丙醇异丁酸酯(![]() )是一种合成香料,其中一种合成路线如图:
)是一种合成香料,其中一种合成路线如图:

已知:R-CH=CH2![]() R-CH2CH2OH。请回答下列问题:
R-CH2CH2OH。请回答下列问题:
(1)A的化学名称是______________,B中含有的官能团名称是________________。
(2)在一定条件下,A与水反应也可以生成B或另外一种生成物,该反应的反应类型为___________,“另外一种生成物”的结构简式为_____________________________。
(3)C可被新制的Cu(OH)2悬浊液氧化,也可以被其他氧化剂所氧化。写出C与银氨溶液反应的化学方程式:_____________________________。
(4)D的核磁共振氢谱显示为6组峰,且峰面积之比为1∶1∶1∶1∶2∶2,则D的结构简式为_______________;D的同分异构体有多种,其中苯环上有两个不含环状的取代基,并能与Na反应的同分异构体有_______种(不含立体异构)。
【答案】 2-甲基-1-丙烯 羟基 加成反应 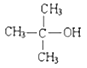
![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O
+2Ag↓+3NH3+H2O ![]() 9
9
【解析】考查有机物的推断和合成,(1)根据苯丙醇异丁酸酯的结构简式,以及合成路线,E为(CH3)2CHCOOH,F为C6H5CH2CH2CH2OH,C生成H,是醛基被氧化成羧基,即C的结构简式为(CH3)2CHCHO,B→C发生醇的氧化反应,即B的结构简式为(CH3)2CHCH2OH,根据信息,A的结构简式为CH2=C(CH3)CH3,名称为2-甲基-1-丙烯;B的官能团是羟基;(2)根据信息,此反应是加成反应,羟基加成到氢原子少的不饱和碳原子上,氢原子加成到氢原子多的不饱和碳原子上,即结构简式为: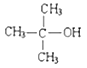 ;(3)银氨溶液把醛基氧化,反应方程式为
;(3)银氨溶液把醛基氧化,反应方程式为![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O ;(5)峰面积之比代表不同化学环境的氢原子个数的比值,D通过与氢气发生加成反应生成E,以及峰面积的比值,即D的结构简式为:
+2Ag↓+3NH3+H2O ;(5)峰面积之比代表不同化学环境的氢原子个数的比值,D通过与氢气发生加成反应生成E,以及峰面积的比值,即D的结构简式为:![]() ;能与金属钠反应,说明含有羟基,D的结构简式种含有两个双键,即同分异构体中有一个碳碳叁键,因此结构简式为
;能与金属钠反应,说明含有羟基,D的结构简式种含有两个双键,即同分异构体中有一个碳碳叁键,因此结构简式为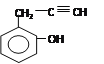 (邻间对三种)、
(邻间对三种)、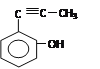 (邻间对三种)、
(邻间对三种)、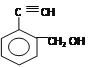 (邻间对三种),羟基不能与碳碳双键或叁键共用一个碳原子,这样结构不稳定,因此符合条件的,共有9种。
(邻间对三种),羟基不能与碳碳双键或叁键共用一个碳原子,这样结构不稳定,因此符合条件的,共有9种。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】氯碱厂电解精制的饱和食盐水,利用电解产品可制取漂白粉等。
(1)如果粗盐中含有SO42﹣,精制时须添加试剂除去SO42﹣,该试剂不能选用______。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)电解饱和食盐水发生的化学方程式_________________。
(3)利用氯气和氢氧化钠溶液制取“84”消毒液的化学方程式____________。
(4)漂白粉在空气中久置后会变质的化学方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种绿色能源,是机动车燃油的最佳替代品。请回答下列有关问题:
(1)用CO可以合成甲醇。已知:
ⅰ.CH3OH(g)+ ![]() O2(g)=CO2(g)+2H2O(l) △H=-764.5 kJmol-1;
O2(g)=CO2(g)+2H2O(l) △H=-764.5 kJmol-1;
ⅱ.CO(g)+ ![]() O2(g)=CO2(g) △H=-283.0 kJmol-1;
O2(g)=CO2(g) △H=-283.0 kJmol-1;
ⅲ.H2(g)+ ![]() O2(g)=H2O(g) △H=-285.8 kJmol-1;
O2(g)=H2O(g) △H=-285.8 kJmol-1;
则 CO(g)+2H2(g)![]() CH3OH(g) △H=________kJ·mol-1。
CH3OH(g) △H=________kJ·mol-1。
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
ⅳ.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-53.7 kJmol-1平衡常数 K1;
CH3OH(g)+H2O(g) △H=-53.7 kJmol-1平衡常数 K1;
ⅴ.CO2(g)+H2(g)![]() CO(g)+H2O(g)△H=+41.2 kJmol-1平衡常数K2。
CO(g)+H2O(g)△H=+41.2 kJmol-1平衡常数K2。
下列四组实验,若控制CO2和H2初始投料比均为1∶2.2,经过相同反应时间测得如下实验数据:
温度(K) | 催化剂 | CO2转化率(%) |
543 | Cu/ZnO纳米棒材料 | 12.3 |
543 | Cu/ZnO纳米片材料 | 10.9 |
553 | Cu/ZnO纳米棒材料 | 15.3 |
553 | Cu/ZnO纳米片材料 | 12.0 |
①CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=___________(用含K1、K2的表达式表示)。
CH3OH(g)的平衡常数K=___________(用含K1、K2的表达式表示)。
②有利于提高CO2转化为CH3OH平衡转化率的措施有_________。
a.使用Cu/ZnO纳米棒衬料
b.使用Cu/ZnO纳米片材料
c.降低反应温度
d.保持投料比不变,增加反应物的浓度
e.增大CO2和H2的初始投料比
③由表格中的数据可知,相同温度下不同的催化剂对CO2的转化率不同,造成该结果的原因是_________________________________________。
(3)甲醇燃料电池是目前技术最成熟,应用最广泛的一种燃料电池,其工作原理如下图所示:

①a气体的名称是_________。
②甲池所在电极为原电池的______极,其电极反应式为__________________________。
③电解液中,H+的移动方向为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯氧化铁是现代电子工业的重要材料。以下是用硫酸厂产生的烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁(软磁a-Fe2O3)的生产流程示意图:

(1)酸浸时,常需将烧渣粉碎、并加入过量H2SO4,其目的是____ ;滤渣的主要成分为 _____(填化学式)。
(2)加入FeS2时,发生反应②的离子方程式为___________。
(3)加入NH4HCO3目的是__________________。“沉淀”时,pH不宜过高,否则制备的FeCO3中可能混有的杂质是_________________。检验FeCO3是否洗涤干净的方法是_____________。
(4)煅烧时,发生反应④的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有Na2SO4、NaHCO3的NaCl固体提纯,制得纯净的氯化钠溶液,某学生设计了如下图所示的实验方案:

已知碳酸氢钠在加热条件下能分解成碳酸钠、二氧化碳和水,而NaCl和Na2SO4固体加热时不发生化学变化。请回答下列问题:
(1)操作①盛放药品可选用___________(填仪器名称)。
(2)操作②为什么不用Ba(NO3)2溶液,其理由是:___________________________。
(3)进行操作②后,判断SO42-已除尽的方法是:______________________________。
(4)操作③的目的是:____________________________________________________。
(5)此设计方案是否严密___________(填“是”或“否”)理由_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com