
光导纤维被认是20世纪最伟大的发明之一,它使信息高速公路在全球迅猛发展。光导纤维的主要成分是
A.CaCO3 B.Si C.SiO2 D.SiC
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:
0.1 mol/L HF溶液的pH=2,则该溶液中有关浓度关系式不正确的是( )
A.c(H+)>c(F-) B.c(H+)>c(HF)
C.c(OH-)>c(HF) D.c(HF) >c(F-)
>c(F-)
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A. | 用热的纯碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| B. | 源白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C. | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与HN4Cl反应生成氨气会降低肥效 |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液中置换出铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
H2SO3是二元弱酸,NaHSO3溶液呈酸性。在0.1 mol·L-1 NaHSO3溶液
中,下列关系正确的是( )
A.c(HSO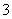 )>c(SO
)>c(SO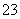 )>c(H2SO3)
)>c(H2SO3)
B.c(Na+)=c(HSO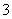 )+2c(SO
)+2c(SO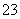 )+c(H2SO3)
)+c(H2SO3)
C.c(Na+)=c(HSO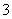 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.c(Na+)+c(H+)=c(HSO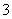 )+c(OH-)+c(SO
)+c(OH-)+c(SO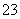 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备
活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
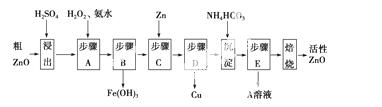
已知:几种离子生成氢氧化物沉淀时的pH如表:
| 待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是_____________________________________
________________________________________________________________________,
该步骤需控制溶液pH的范围是_____________________________________________。
(2)A溶液中主要含有的溶质是____________。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进 行的原因是ΔS________(选填“=”、“>”或“<”)0。
行的原因是ΔS________(选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为________mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,只能表示一个化学反应的是
①Zn+Cu2+ ==Zn2++Cu ②Ag++Cl-== AgCl↓
③Cl2+H2O H++Cl-+HClO ④CO32-+2H+ == CO2↑+H2O
H++Cl-+HClO ④CO32-+2H+ == CO2↑+H2O
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:I2+2S2O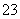 ===S4O
===S4O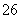 +2I-
+2I-
相关物质的溶度积常数见下表:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl2 | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入________,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是____________________________(用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是____________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20 .00 mL。
.00 mL。
①可选用_____作滴定指示剂,滴定终点的现象是__________。
②CuCl2溶液与KI反应的离子方程式为___________________。
③该试样中CuCl2·2H2O的质量百分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,浓度均为0.1 mol·L-1的三种溶液:①醋酸 ②氢氧化钠 ③醋酸钠,下列说法不正确的是( )
A.c(CH3COO-):③>①
B.水电离出的c(OH-):②>①
C.①和②等体积混合后的溶液:c(OH-)=c(H+)+c(CH3COOH)
D.①和③等体积混合后的溶液:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com