
| A. | 1molNa2O2所含的阴离子数 | |
| B. | 22.4LCO2所含氧原子数 | |
| C. | 2L1mol•L-1硫酸溶液中所含的氢离子数 | |
| D. | 点燃条件下,1molCl2与足量的钠充分反应时转移的电子数 |
分析 A.过氧化钠是钠离子和过氧根离子构成;
B.气体摩尔体积是指标准状况下1mol气体所占体积为22.4L;
C.n=CV=$\frac{N}{{N}_{A}}$,溶液中水电离出氢离子和氢氧根离子;
D.氯气和钠反应生成氯化钠,电子转移依据反应的氯气计算;
解答 解:A.过氧化钠是钠离子和过氧根离子构成,1molNa2O2所含的阴离子数为NA,故A错误;
B.气体摩尔体积是指标准状况下1mol气体所占体积为22.4L,温度压强不知,22.4LCO2所含物质的量不能计算,不能计算所含氧原子数,故B错误;
C.n=CV=$\frac{N}{{N}_{A}}$,2L1mol•L-1硫酸溶液中硫酸电离出的氢离子物质的量=2L×1mol/L×2=4mol,所含的氢离子数溶液中水电离出氢离子和氢氧根离子,溶液中氢离子数>4NA,故C错误;
D.氯气和钠反应生成氯化钠,电子转移依据反应的氯气计算,1molCl2与足量的钠充分反应,Cl2~2Cl-~2e-,反应时转移的电子数2NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的计算应用,主要是物质结构、气体体积、溶质物质的量、氧化还原反应电子转移的分析与计算,题目难度中等.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 单质硅可用于制造光纤制品 | B. | 碳酸氢钠常用于焙制糕点 | ||
| C. | 氧化铝可用于制造耐火坩埚 | D. | 氢氧化铝常用于治疗胃酸过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水保存在无色玻璃瓶中 | |
| B. | 氢气在氯气中燃烧生成白色烟雾 | |
| C. | 常温下,浓硝酸可用铝罐来贮存,说明浓硝酸具有强氧化性 | |
| D. | 向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有吸水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验数据或现象 | 结论 | |
| A | 用PH计分别测定SO2和CO2饱和溶液的PH | 前者PH小 | H2SO3酸性强于H2CO3 |
| B | 向Ag Cl悬浊液中加入NaI溶液 | 产生黄色沉淀 | Ksp(AgI)>Ksp(AgCl) |
| C | 向滴用酚酞的氨水中加入少量CH3COONH4固体 | 溶液红色变浅 | 氨水中存在电离平衡 |
| D | 等体积、等PH的HA和HB两种酸溶液分别与足量的锌反应 | 相同时间内,HA酸产生的氢气多 | HA是强酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
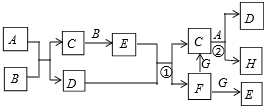 下列有关物质的转化关系如图所示(部分物质与条件已略去,其中反应②的条件是“700℃,催化剂”).G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体.请回答下列问题:
下列有关物质的转化关系如图所示(部分物质与条件已略去,其中反应②的条件是“700℃,催化剂”).G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体.请回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
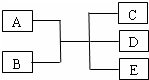 已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系.
已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com