
 北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”.有一种有机物的键线式也酷似牛,如图所示,故称为牛式二烯炔醇.下列有关说法不正确的是( )
北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”.有一种有机物的键线式也酷似牛,如图所示,故称为牛式二烯炔醇.下列有关说法不正确的是( )| A. | 牛式二烯炔醇含有3种官能团 | |
| B. | 牛式二烯炔醇分子内能发生消去反应 | |
| C. | 1 mol牛式二烯炔醇最多可与6 molBr2发生加成反应 | |
| D. | 牛式二烯炔醇可发生取代反应 |
分析 A.该物质中含有醇羟基、碳碳双键、碳碳三键;
B.该物质中醇羟基不能发生消去反应;
C.碳碳双键和碳碳三键能与溴发生加成反应;
D.醇羟基可以发生取代反应.
解答 解:A.该物质中含有醇羟基、碳碳双键、碳碳三键,所以有三种官能团,故A正确;
B.该物质中连接醇羟基碳原子相邻碳原子上不含氢原子,所以醇羟基不能发生消去反应,故B错误;
C.碳碳双键和碳碳三键能与溴发生加成反应,1 mol牛式二烯炔醇最多可与6 molBr2发生加成反应,故C正确;
D.醇羟基具有醇的性质,可以发生取代反应,故D正确;
故选B.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查醇、炔、烯的性质,注意该醇羟基不能发生消去反应,易错选项是B.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③④ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是两种核素 | B. | 互为同素异形体 | ||
| C. | 中子数分别为176和177 | D. | 电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 平均风速(m/s) 天气情况 | 空气中SO2的平均含量(mg/L) |
| 雨前 | 0.03 |
| 雨后 | 0.01 |
| 晴 | 0.015 |
| 晴 | 0.03 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g苯中含有碳碳双键数目为0.3NA | |
| B. | 1mol的羟基(-OH)所含电子的数目为9NA | |
| C. | 25℃时,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| D. | 1.0L 1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)/c(OH-)=1012的溶液中:NH${\;}_{4}^{+}$、Al3+、NO${\;}_{3}^{-}$、Cl- | |
| B. | 由水电离的c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、F- | |
| C. | pH=7的溶液中:K+、CO32-、SO42-、Cl- | |
| D. | pH=1的溶液中:Fe2+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
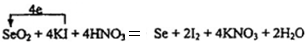 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com