

 ��
�� ��
�� ��һ����Ҫ��ҩ��ϳ��м��壬������Ŀ������Ϣ��
��һ����Ҫ��ҩ��ϳ��м��壬������Ŀ������Ϣ�� Ϊԭ���Ʊ��û�����ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�H2C�TCH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH��
Ϊԭ���Ʊ��û�����ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�H2C�TCH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH�� ���� ���ݺϳ���·��֪��E������Cu��OH ��2���������·�Ӧ���ữ���F��E�к���ȩ������E�Ľṹ��ʽΪ�� ��D����������E����D�Ľṹ��ʽΪ��
��D����������E����D�Ľṹ��ʽΪ�� ��Cˮ������D����C�Ľṹ��ʽΪ��
��Cˮ������D����C�Ľṹ��ʽΪ��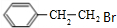 ��F��CH3CH2OH��Ũ������������£�����������Ӧ���ɵ�G����G�Ľṹ��ʽΪ
��F��CH3CH2OH��Ũ������������£�����������Ӧ���ɵ�G����G�Ľṹ��ʽΪ ��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����I�Ľṹ��ʽΪ��
��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����I�Ľṹ��ʽΪ�� ���ݴ˽��н��
���ݴ˽��н��
��� �⣺���ݺϳ���·��֪��E������Cu��OH ��2���������·�Ӧ���ữ���F��E�к���ȩ������E�Ľṹ��ʽΪ�� ��D����������E����D�Ľṹ��ʽΪ��
��D����������E����D�Ľṹ��ʽΪ�� ��Cˮ������D����C�Ľṹ��ʽΪ��
��Cˮ������D����C�Ľṹ��ʽΪ��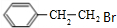 ��F��CH3CH2OH��Ũ������������£�����������Ӧ���ɵ�G����G�Ľṹ��ʽΪ
��F��CH3CH2OH��Ũ������������£�����������Ӧ���ɵ�G����G�Ľṹ��ʽΪ ��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����IΪ��
��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����IΪ�� ��
��
��1������H�Ľṹ��ʽ��֪��H���еĹ�����Ϊȩ������������Ӧ3Ϊ�ǻ���ȥ����̼̼˫����
�ʴ�Ϊ��ȩ���������� ��ȥ��Ӧ��
��2����Ӧ1Ϊ�ӳɷ�Ӧ���Ƚ�A��B�Ľṹ��֪��XΪCH��CH��
�ʴ�Ϊ��CH��CH��
��3��F��CH3CH2OH��Ũ������������£�����������Ӧ���ɵ�G��Ӧ�ķ���ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��4�������������������ܷ���������Ӧ��˵����ȩ����������FeCl3������ɫ��Ӧ��˵���з��ǻ����۷����к���5�ֲ�ͬ��ѧ�������⣬�����������F��ͬ���칹��Ϊ ��
��
�ʴ�Ϊ�� ��
��
��5������ͨ����ȥ��Ӧ�õ�̼̼˫������H2O2��������HBr�ӳɣ�Br�ڶ˵��Cԭ���ϣ�ˮ�ⷴӦ����-OH��Ȼ����������Ӧ�����ղ�����Ժϳ�·��ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л��ϳɣ���Ŀ�Ѷ��еȣ������漰�л���Ӧ���͡�ͬ���칹����д���л���Ӧ����ʽ��֪ʶ��ע����ݷ�Ӧ���������ƶϣ���Ҫѧ���������չ����ŵ�������ת������4����ͬ���칹�����дΪ�״��㡢�ѵ㣮


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������������145��Ϳ�ʼ��Ӧ���ڲ�ͬ�¶Ⱥʹ������������ɲ�ͬ�������ͼ����
������������145��Ϳ�ʼ��Ӧ���ڲ�ͬ�¶Ⱥʹ������������ɲ�ͬ�������ͼ����| t/s | 0 | 500 | 1000 |
| c��N2O5��/mol•L-1 | 5.00 | 3.52 | 2.48 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ��Ҫ�ɷ� | Cu | Ag | Au | Se | Te |
| �ٷֺ���/% | 23.4 | 12.1 | 0.9 | 6.7 | 3.1 |
| �̶������¶� | �̶�H2SO4Ũ�� | |||||||||||
| H2SO4Ũ��/mol•L-1 | ������/% | �����¶�/�� | ������/% | |||||||||
| Cu | Ag | Au | Se | Te | Cu | Ag | Au | Se | Te | |||
| 4 | 95.1 | 4.67 | ��0.2 | 0.83 | 8.93 | 30 | 87.1 | 4.58 | ��0.2 | 0.08 | 6.83 | |
| 3 | 94.5 | 4.65 | ��0.2 | 0.28 | 6.90 | 40 | 94.5 | 4.65 | ��0.2 | 0.28 | 6.90 | |
| 2 | 78.1 | 2.65 | ��0.2 | 0.05 | 2.85 | 50 | 96.1 | 5.90 | ��0.2 | 0.64 | 8.73 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�Т٢ڢ� | B�� | ֻ�Т٢� | C�� | ֻ�Тۢܢ� | D�� | ֻ�Тڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ������Ȫʵ�� | B�� | 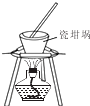 �������ڣ�NaOH�� | ||
| C�� |  ��֤þƬ��ϡ���ᷴӦ���� | D�� | 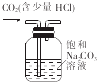 ��ȥCO2�е�����HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| һ��״̬�ķ��� | H2��g�� | Br2��l�� | HBr��g�� |
| 1mol�÷����еĻ�ѧ���������յ�����/kJ | 436 | a | 369 |
| A�� | 404 | B�� | 344 | C�� | 260 | D�� | 200 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ѡ�� | ���ᴿ������ | ���� | �����Լ� | ���ӷ��� |
| A | CO2��g�� | SO2��g�� | ����NaHSO3��Һ��ŨH2SO4 | ϴ�� |
| B | FeCl2��aq�� | Fe3+��aq�� | �������� | ���� |
| C | Na2CO3��s�� | NaHCO3��s�� | �������� | ���� |
| D | Na2CO3��aq�� | NaHCO3��aq�� | ����NaOH��Һ | ϴҺ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ά | B�� | ���� | C�� | �ϳ���ά | D�� | �ϼ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com