
| A. | 原子半径 A>B>D>C | B. | 原子序数 d>c>b>a | ||
| C. | 离子半径 C>D>B>A | D. | 单质的还原性 A>B>D>C |
分析 依据短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则A、B、C、D在元素周期表中的相对位置大致是: ,结合元素在周期表中的位置以及元素周期律的递变规律解答该题.
,结合元素在周期表中的位置以及元素周期律的递变规律解答该题.
解答 解:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,A、B、C、D在元素周期表中的相对位置大致是: ,说明A与B同周期,C与D同周期,且A、B处于C、D的下一周期,所以,原子半径应是B>A>C>D,原子序数应是a>b>d>c,据电子层结构相同,随原子序数增大,离子半径依次减小,推知离子半径应是C>D>B>A,单质的还原性应是B>A>C>D.
,说明A与B同周期,C与D同周期,且A、B处于C、D的下一周期,所以,原子半径应是B>A>C>D,原子序数应是a>b>d>c,据电子层结构相同,随原子序数增大,离子半径依次减小,推知离子半径应是C>D>B>A,单质的还原性应是B>A>C>D.
故选:C.
点评 本题考查原子结构与元素周期律的关系,注意根据离子核外电子排布相同结合离子的结构判断元素在周期表中的位置,为解答该题的关键,题目难度中等.


科目:高中化学 来源: 题型:推断题
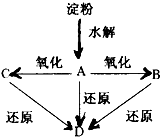 如图所示,淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应.A、B、C都可以被强还原剂还原成为D(C6H14O6).已知,相关物质被氧化的难易次序是:RCHO最易,R-CH2OH次之,
如图所示,淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应.A、B、C都可以被强还原剂还原成为D(C6H14O6).已知,相关物质被氧化的难易次序是:RCHO最易,R-CH2OH次之,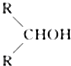 最难.
最难.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃,pH=13的NaOH溶液中含有OH-为0.1NA | |
| B. | 1 L 0.1 mol•L-1 CuSO4溶液中含有Cu2+为0.1NA | |
| C. | 2.24 L N2和NH3混合气体中原子间含有的共用电子对数目为0.3NA | |
| D. | 2 mol SO2和1 mol O2在一定条件下充分反应后,所得混合气体的分子数大于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 化学反应中能量变化的主要原因是物质状态的改变 | |
| B. | 铝与盐酸的反应中,反应物的总能量比生成物的总能量高 | |
| C. | 图I所示的装置能将化学能转变为电能 | |
| D. | 图II所示的反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子数目相等的三种气体,质量最大的是Z | |
| B. | 相同条件下,同质量的二种气体,气体密度最小的是X | |
| C. | 若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1mol | |
| D. | 同温下,体积相同的两容器分别充2 g Y气体和l g Z气体,则其压强比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红棕色的NO2加压后颜色先变深后变浅 | |
| B. | 由氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 | |
| C. | 加入铁触媒做催化剂更有利于工业合成氨 | |
| D. | 锌粒粉碎后与稀硫酸反应产生氢气速度更快 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
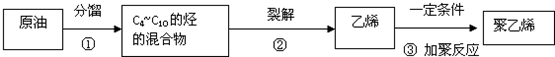
 ,
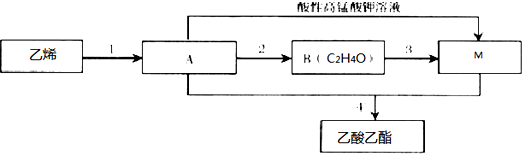
,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com