
��17�֣��ɽ�������PCL�Ľṹ�ɱ�ʾΪ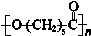 ����ϳ�·�����¡�
����ϳ�·�����¡�
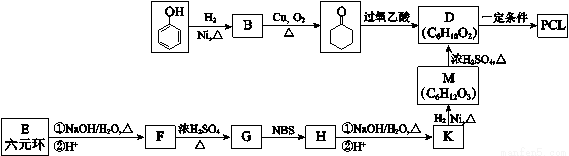
��֪��
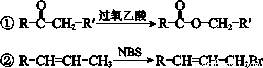
�ش��������⣺
��1��B�����������ŵ�������______��
��2��D�Ľṹ��ʽ��______��
��3��M�ķ��ӽṹ����֧����M����D�ķ�Ӧ������______��
��4��E��D��ͬ���칹�壬������ͬ�Ĺ����š�E�Ľṹ��ʽ��______��
��5��F����G�Ļ�ѧ����ʽ��______��
��6������˵����ȷ����______��
a��Kû��˳���칹
b��M��һ�������¿ɷ����ۺϷ�Ӧ
c��PCL�Ľṹ�к�������
��7��H����������������Һ��Ӧ�Ļ�ѧ����ʽ��______��
��8��M���������Z�����Ǻϳ�������ԭ��֮һ����B��ԭ�Ͽ��Ƶü����ᣬ���������Ϣ�����ϳ�·������ͼ�����Լ���ѡ����______��
��֪��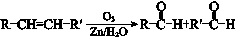
�ϳ�·������ͼʾ����
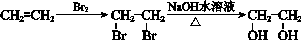
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��һ3���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��һδ֪Ũ�ȵ�ϡ����25mL���ȼ���25mL5mol/LBaCl2��Һ�ļ�NaOH��Һ�������ȥ1.0mol/LNaOH��Һ25mLǡ����ȫ�к͡���ϡ��������ʵ���Ũ��Ϊ
A��0.5mol/L B��1.0mol/L C��1.5mol/L D��2.0mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���к���������һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ʒ����Ҫ�ɷּ�����;��Ӧ����ȷ����
A | B | C | D | |
��Ʒ |
|
|
|
|
��Ҫ�ɷ� | (NH4)2SO4 | NaHCO3 | Si | Fe2O3 |
��; | ���� | ����� | ���� | Ϳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ˮ�и�����ѧ�ڶ�ģ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
(15��)�������[KMnO4]�dz��õ�����������ҵ�������̿�(��Ҫ�ɷ���MnO2)Ϊԭ���Ʊ�������ؾ��塣�м����Ϊ�����[K2MnO4]����ͼ��ʵ����ģ���Ʊ��IJ������̣�
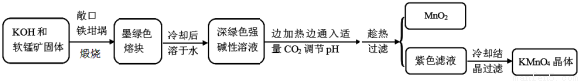
������ϣ�
�������ܽ��
���� | KMnO4 | K2CO3 | KHCO3��] | K2SO4 | CH3COOK |
20���ܽ�� | 6.4 | 111 | 33.7 | 11.1 | 217 |
�������[K2MnO4]
�����״��ī��ɫ�ᾧ����ˮ��Һ������ɫ�����������(MnO42��)��������ɫ��
��ѧ���ʣ���ǿ������Һ���ȶ��������ԡ����Ժ������Ի����£�MnO42���ᷢ���绯��Ӧ��
�Իش��������⣺
��1���������̿��KOH����ʱ��������ʯӢ������ѡ����������������______________��
ʵ���������������ձ�¶�ڿ����еĹ����������Ӧ�Ļ�ѧ����ʽΪ_______��
��2��ʵ��ʱ����CO2����������KHCO3�����µõ���KMnO4��Ʒ�Ĵ��Ƚ��͡���д��ʵ����ͨ������CO2ʱ��ϵ�п��ܷ�����Ӧ���ӷ���ʽ �� ��
����������ԭ��Ӧ���������ͻ�ԭ����������Ϊ_________________________��
��3������CO2��ͨ�������ѿ��ƣ���˶�����ʵ�鷽�������˸Ľ�������ʵ����ͨCO2��Ϊ���������ᡣ�������Ϸ�����ѡ����������________ ���õ��IJ�Ʒ���ȸ��ߡ�
A������ B��Ũ���� C��ϡ����
��4����ҵ��һ����ö��Ե缫����������Һ��ȡ������أ���д���õ�ⷴӦ�Ļ�ѧ����Ϊ_________��
��ͳ���ղ�����Ĥ��ⷨ���ڸ���Ӧ������MnԪ�������ʺ͵���Ч�ʶ���ƫ�͡���ͬѧ���뵽���ӽ���Ĥ����ⱥ��ʳ��ˮ����Ľ����������������ӽ���Ĥ�ָ����������е��(��ͼ)��
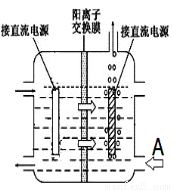
ͼ��A�ڼ������Һ���Ϊ__________��
ʹ�������ӽ���Ĥ�������MnԪ�������ʵ�ԭ��Ϊ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ˮ�и�����ѧ�ڶ�ģ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڹ��������������ȷ����(NA��ʾ����٤������)
A��7.8 g�������ƺ��еĹ��õ��Ӷ���Ϊ0.2NA
B��2H2O2(l)=2H2O(l)��O2(g) ��H=98.2 kJ��mol1����S=70.5 J��mol1��K1���÷�Ӧ�������Է�����
C����������ʹ���������Һ��ɫ��1 mol��������õ�2NA����
D���ں���NH4�� ��Ba2����Cl����NO3�����ӵ���Һ �������������������ϸ�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱����������������ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���н�����ʵ�Ļ�ѧ����ʽ����ȷ����
A���������ڿ����м��ȣ����ɵ���ɫ���壺2Na��O2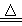 Na2O2
Na2O2
B������������Һ�м��백ˮ�Ʊ�����������Al3+��3NH3H2O=Al��OH��3����3NH4+
C�����ڳ�ʪ�Ļ��������⣺3Fe��4H2O= Fe3O4��4H2��
D��������������ˮ���������ɣ�3NO2��H2O=2HNO3��NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���к����������ڶ�ѧ����ĩ��ϰ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������£�ͨ�����з�Ӧ��ʵ��ȼú��������Ļ��գ�����Y�ǵ��ʡ�
SO 2(g) + 2CO(g)  2X(g)+Y(l)
2X(g)+Y(l)
Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶����ó��������崫������ò�ͬʱ���SO2��COŨ�����±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 |
c(SO2)/mol��L-1 | 1.00 | 0.50 | 0.23 | 3.00��10-37 | 3.00��10-37 |
c(CO)/mol��L-1 | 4.00 | 3.00 | 2.46 | 2.00 | 2.00 |
����˵������ȷ����
A��X�Ļ�ѧʽΪCO2
B��ǰ1s��v(X)= 1.00 mol��L-1��s-1
C���û���ԭ��������SO 2�Ļ�ԭ��
D�����¶��£��˷�Ӧ��ƽ�ⳣ������ֵ��3.33��1036
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱���к���������4��ģ����ϰ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���н�����ʵ�ķ���ʽ����ȷ����
A�����Ȼ�����Һ�еμӹ�����ˮ�����ɰ�ɫ��״������Al3++ 3NH3��H2O=Al(OH)3��+ 3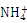
B������������������þ�Գ�ȥ�Ȼ�þ��Һ�е������Ȼ�����Fe3+ + 3OH��=Fe(OH)3��
C��������0.1mol/L �Ȼ����ҺpH=5��NH4++H2O 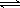 NH3��H2O+ H+
NH3��H2O+ H+
D����⾫��ͭʱ����ͭ�ܡ�������
Cu-2e��=Cu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�߶�4���¿���ѧ�Ծ��������棩 ���ͣ�������
ij�����л���A��̼���⡢������Ԫ����ɣ���ȡ3g A��4.48L��������״�������ܱ�������ȼ�գ�ȼ�պ����ɶ�����̼��һ����̼��ˮ���������跴Ӧ��û��ʣ�ࣩ������Ӧ���ɵ���������ͨ��Ũ����ͼ�ʯ�ң�Ũ��������3.6g����ʯ������4.4g���ش��������⣺
��1��3gA��������Ԫ�غ�̼Ԫ�ص����ʵ������Ƕ��٣�
��2��ͨ������ȷ�����л���ķ���ʽ��
��3�����˴Ź��������г��������źŷ壬��ǿ��֮��Ϊ3:3:2����д�����л���Ľṹ��ʽ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com