
| 实验编号 | 0.01mol?L-1 酸性KMnO4溶液 |
0.1mol?L-1 H2C2O4溶液 |
水 | 1mol?L-1 MnSO4溶液 |
反应温度/℃ | 反应时间 |
| I | 2ml | 2ml | 0 | 0 | 20 | 125 |
| II | 1ml | 0 | 20 | 320 | ||
| III | 0 | 50 | 30 | |||
| IV | 2ml | 2ml | 0 | 2滴 | 20 | 10 |
| II | 2 | 1 | |
III |
2 | 2 | 0 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、稀醋酸和稀氨水反应 |
| B、稀硫酸和烧碱溶液反应 |
| C、稀盐酸和氢氧化铜反应 |
| D、稀硫酸和氢氧化钡溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | Na2CO3可与盐酸反应 | 纯碱可用于治疗胃病 | Ⅰ对,Ⅱ对,有 |
| B | Cl2使鲜艳的红色花瓣褪色 | Cl2具有漂白性 | Ⅰ对,Ⅱ对,有 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
| D | Na2O2能和CO2、H2O反应生成O2 | 过氧化钠可用作航天员的供氧剂 | Ⅰ对,Ⅱ对,有 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4 L CO2和O2混合气体中含有的氧原子数约为NA |
| B、300 mL 2 mol?L-1蔗糖溶液中所含分子数为0.6 NA |
| C、1 L 1 mol?L-1的K2CO3溶液中离子总数大于3NA |
| D、常温常压下,2.24 L四氯化碳中所含氯原子数约小于0.4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
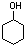 )是一种有机化工基础原料,工业上的主要合成途径及有关反应如下:
)是一种有机化工基础原料,工业上的主要合成途径及有关反应如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
 用右图表示的一些物质或概念之间的从属或包含关系中不正确的是( )
用右图表示的一些物质或概念之间的从属或包含关系中不正确的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 苯 | 芳香烃 | 有机化合物 |
| B | 溶液 | 分散系 | 混合物 |
| C | 强电解质 | 电解质 | 化合物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=0的溶液中:Ca2+、Al3+、ClO-、Cl- |
| B、含有大量AlO2-的溶液中:K+、Ca2+、Br-、HCO3- |
| C、加入Mg能放出H2的溶液中:Na+、NH4+、Cl-、SO42- |
| D、酚酞显无色的溶液中:K+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com