
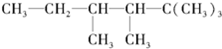
 ,5号碳原子上没有H原子,与相连接T原子不能形成碳碳双键,能形成双键位置有:1和2之间;2和3之间;3和4之间,3和6之间,4和7之间,故该烃共有5种结构;
,5号碳原子上没有H原子,与相连接T原子不能形成碳碳双键,能形成双键位置有:1和2之间;2和3之间;3和4之间,3和6之间,4和7之间,故该烃共有5种结构; ,所以能形成三键位置有:1和2之间,此炔烃的结构简式可能为
,所以能形成三键位置有:1和2之间,此炔烃的结构简式可能为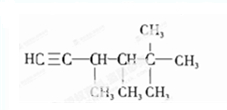 ;
; .
.

科目:高中化学 来源: 题型:
| A、绿色化学的核心是对环境污染进行综合治理 | B、烟、云、雾在阳光照射下可观察到丁达尔现象 | C、“温室效应”、“酸雨”的形成都与氮氧化合物有关 | D、高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该烃的名称:2-乙基-1-丁烯 | B、该烃与氢气加成得到的烷烃的名称:3-甲基戊烷 | C、该烃能使溴的四氯化碳溶液褪色,不能与溴发生取代反应 | D、该烃能在一定条件下与HCl加成,得到两种卤代烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | 氢气 | 甲烷 | 乙烯 | 丙烯 |
| 质量分数(%) | 20 | 56 | 14 | 10 |
| A、5.63 | B、7.02 |
| C、7.41 | D、10.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙烯分子中所有原子位于同一平面 | B、丙烯分子中不存在同分异构体 | C、丙烯分子中最多有7个原子位于同一平面 | D、丙烯分子中3个碳原子在同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
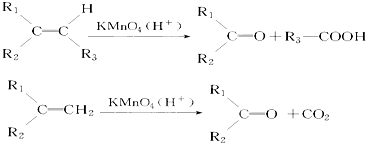
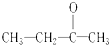 ),则此烯烃的结构简式是
),则此烯烃的结构简式是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无水醋酸铯的化学式为CH3COOCs,易溶于水,其水溶液显碱性 | B、碳酸氢铯加热即分解生成碳酸铯、二氧化碳和水 | C、在Na、K、Rb、Cs中,Cs熔点最高,密度最大 | D、CsH是离子化合物,与水反应可以生成H2 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省海珠等四区高三联考理综化学试卷(解析版) 题型:选择题
短周期元素R、T、Q、W在元素周期表中的相对位置如下图所示,其中Q单质可制成半导体材料。下列判断正确的是
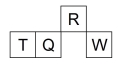
A.W形成的离子半径大于T形成的离子半径
B.W的单质在过量氧气中燃烧生成WO3
C.最高价氧化物的水化物的酸性:R<Q
D.T是地壳中含量最多的金属元素,其单质的化学性质较活泼
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com