
| A. | ①③④⑥⑦ | B. | 除外②都是 | C. | ①④⑥⑦ | D. | ①③④⑦ |
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和浓硫酸加热至140℃反应:2CH3CH2OH$\stackrel{140℃}{→}$CH3CH2OCH2CH3+H2O | |
| B. | 溴乙烷与NaOH醇溶液加热反应:CH3CH2Br+NaOH$→_{△}^{醇}$CH2═CH2↑+NaBr | |
| C. | 苯酚钠溶液中通少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH↓+HCO3- | |
| D. | 乙醛溶液与银氨溶液共热:2CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$2CH3COONH4+2Ag↓+3NH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 存在于O2、SO2和SO3中 | B. | 只存在于O2和SO3中 | ||
| C. | 只存在于O2和SO2中 | D. | 只存在于O2中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
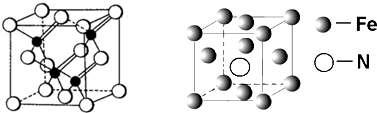
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,元素Z在周期表中的位置是第三周期ⅣA族.
,元素Z在周期表中的位置是第三周期ⅣA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加强废旧塑料的回收与利用,能有效地治理白色污染 | |
| B. | 合成塑料、合成纤维、合成橡胶是三大合成材料 | |
| C. | 线型结构的塑料具有热塑性 | |
| D. | 塑料、纤维素、蛋白质、天然橡胶属于天然高分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
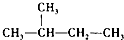 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
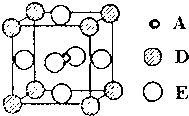 A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数逐渐增大.A原子核外电子有6种不同的运动状态,C的基态原子2p能级上有2个未成对电子,C2-离子与D2+离子具有相同的电子层结构,E的基态原子的外围电子排布式为3d84s2.
A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数逐渐增大.A原子核外电子有6种不同的运动状态,C的基态原子2p能级上有2个未成对电子,C2-离子与D2+离子具有相同的电子层结构,E的基态原子的外围电子排布式为3d84s2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com