
·ÖĪö £Ø1£©øł¾Ż14.51æĖ°×É«³ĮµķŹĒBaCO3ŗĶBaSO4»ģŗĻĪļ£¬BaSO4²»ČÜÓŚĖ®£¬æÉÖŖBaCO3ŗĶBaSO4µÄÖŹĮ棬Na2SO4µÄĪļÖŹµÄĮæµČĶ¬ÓŚBaSO4µÄĪļÖŹµÄĮ棬Na2CO3µÄĪļÖŹµÄĮæµČĶ¬ÓŚBaCO3µÄĪļÖŹµÄĮ棬ŅŌ“Ė·Ö±š¼ĘĖćŅŌ“Ė¼ĘĖćŌ»ģŗĶČÜŅŗÖŠNa2CO3ŗĶNa2SO4µÄĪļÖŹµÄĮæÅØ¶Č£¬ŅŌ¼°²śÉśµÄĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»ż£»
£Ø2£©øł¾Ż·½³ĢŹ½BaCO3+2HNO3ØTØTBa£ØNO3£©2+CO2”ü+H2O²¢ÓÉ£Ø1£©ÖŠBaCO3µÄĪļÖŹµÄĮæĒóµĆĻūŗÄHNO3µÄĪļÖŹµÄĮ棬øł¾ŻĢāŅāĒó³öĻõĖįµÄÖÖĪļÖŹµÄĮ棬Į½ÕßĻą¼õ¼ČµĆŹ£ÓąĻõĖįµÄĪļÖŹµÄĮ棬²¢øł¾Żn=cv£¬ĒóH+µÄÅØ¶Č²¢ĒópH£®
½ā“š ½ā£ŗ£Ø1£©Ģ¼Ėį±µÄܹ»ČÜÓŚĻ”ĻõĖį£¬ĮņĖį±µ²»ČÜ£¬ŅĄ¾ŻÖŹĮæŹŲŗćµĆ£ŗn£ØNa2SO4£©=n£ØBaSO4£©=$\frac{4.66g}{233g/mol}$=0.02mol£¬ĖłŅŌĮņĖįÄʵÄĪļÖŹµÄĮæÅضČĪŖ£ŗc£ØNa2SO4£©=$\frac{0.02mol}{0.5L}$=0.04mol/L£»
Ģ¼Ėį±µµÄÖŹĮæĪŖ£ŗ14.51g-4.66g=9.85g£¬Ģ¼Ėį±µµÄĪļÖŹµÄĮæĪŖn£ØBaCO3£©=$\frac{9.85g}{197g/mol}$=0.05mol£¬øł¾ŻÖŹĮæŹŲŗćæÉÖŖ£ŗn£ØNa2CO3£©=n£ØBaCO3£©=0.05mol£¬ŌņĢ¼ĖįÄʵÄĪļÖŹµÄĮæÅضČĪŖ£ŗc£ØNa2CO3£©=$\frac{0.05mol}{0.5L}$=0.1mol/L£¬
“š£ŗŌ»ģŗĻČÜŅŗÖŠNaCO3ŗĶNa2SO4µÄĪļÖŹµÄĮæÅØ¶Č·Ö±šĪŖ0.04mol/L”¢0.1mol/L£®
£Ø2£©Éč·“Ó¦ĻūŗÄĻõĖįµÄĪļÖŹµÄĮæĪŖxmol£®
BaCO3+2HNO3ØTØTBa£ØNO3£©2+CO2”ü+H2O
1mol 2mol
0.05mol xmol
$\frac{1mol}{0.05mol}$=$\frac{2mol}{xmol}$£¬x=0.1mol
¼“n£ØĻūŗÄHNO3£©=0.1mol
”ßn£ØŌHNO3£©=0.1L”Į2mol=0.2mol
”ąn£ØŹ£HNO3£©=n£ØŌHNO3£©-n£ØĻūŗÄHNO3£©=0.2mol-0.1mol=0.1mol
c£ØŹ£HNO3£©=c£ØH+£©=$\frac{n£ØĻūŗÄHNO3£©}{V}$=$\frac{0.1mol}{0.1L}$=1mol
pH=-lgc£ØH+£©=-lg1=0
“š£ŗĻ”ŹĶŗóČÜŅŗµÄpHĪŖ0
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ¹Ų·½³ĢŹ½µÄ¼ĘĖć£¬Ć÷Č··“Ó¦µÄŹµÖŹŹĒ½āĢā¹Ų¼ü£¬×¢ŅāĢ¼Ėį±µŗĶĮņĖį±µµÄŠŌÖŹ£¬²¢ĒŅÓÉŹ£ÓąĻõĖįµÄÅØ¶ČĄ“ĒóČÜŅŗµÄpH£¬±¾ĢāÄæÄŃ¶Č²»“ó£®ÉłĆ÷£ŗ±¾ŹŌĢā½āĪöÖų×÷ČØŹōŻ¼ÓÅĶųĖłÓŠ£¬Ī“¾ŹéĆęĶ¬Ņā£¬²»µĆø“ÖĘ·¢²¼£®ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
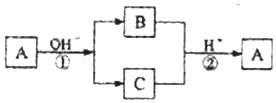
| A£® | XŌŖĖŲæÉÄÜĪŖAl | B£® | XŌŖĖŲæÉÄÜĪŖ½šŹō£¬Ņ²æÉÄÜĪŖ·Ē½šŹō | ||
| C£® | ·“Ó¦¢ŁŗĶ¢Ś»„ĪŖæÉÄę·“Ó¦ | D£® | ·“Ó¦¢ŁŗĶ¢ŚŅ»¶ØĪŖŃõ»Æ»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 150 mL 2 mol•L-1µÄNaCl | B£® | 75 mL 2 mol•L-1µÄNH4Cl | ||
| C£® | 150 mL 3 mol•L-1µÄKCl | D£® | 75 mL 2 mol•L-1µÄCaCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŻĮæĘæĪ“øÉŌļ | |
| B£® | ¶ØČŻŹ±ø©ŹÓŅŗĆę | |
| C£® | ×ŖŅĘŹ±ÓŠŅŗĢ彦³ö | |
| D£® | µßµ¹Ņ”ŌČŗó·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ŌŁ¼ÓĖ®ÖĮæĢ¶ČĻß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
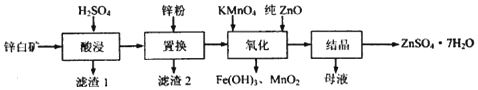
| ½šŹōĄė×Ó | æŖŹ¼³ĮµķµÄpH | ³ĮµķĶźČ«µÄpH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 6.4 | 8.0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com