
| A£® | amol | B£® | bmol | C£® | £Ø3a-b£©mol | D£® | £Øa+b£©mol |
·ÖĪö ¶žĮņ»ÆĢ¼£ØCS2£©Äܹ»ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶSO2£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCS2+3O2=CO2+2SO2£»ŅĄ¾Ż·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæµÄ±ä»Æ¼ĘĖćÅŠ¶Ļ£®
½ā“š ½ā£ŗ¶žĮņ»ÆĢ¼£ØCS2£©Äܹ»ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶSO2£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCS2+3O2=CO2+2SO2£»¶žĮņ»ÆĢ¼£ØCS2£©ŹĒŅŗĢ壬·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæĪŖŃõĘųµÄĪļÖŹµÄĮ棬ĖłŅŌ·“Ó¦ŗóµÄĘųĢåĪļÖŹµÄĮæĪŖbmol£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·½³ĢŹ½µÄ¼ĘĖć£¬Ö÷ŅŖæ¼²éĮĖ·“Ó¦Ē°ŗóµÄĘųĢåĢå»ż±ä»ÆĢŲÕ÷£¬²»Šč¼ĘĖćøł¾Ż·“Ó¦ĢŲÕ÷Ö±½ÓÅŠ¶Ļ£¬½Ļ¼ņµ„£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ²½Öč | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó¼°Źż¾Ż |
| ¢Ł | Č”wgM·ŪÄ©ČÜÓŚ¹żĮæµÄŃĪĖį | ²śÉśĘųĢåXŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ224mL£¬²¢µĆµ½ĪŽÉ«ČÜŅŗ |
| ¢Ś | Ļņ²½Öč¢ŁĖłµĆµÄČÜŅŗÖŠµĪ¼Ó°±Ė®£¬µ÷½ŚpHÖĮ6£¬¹żĀĖ”¢Ļ“µÓ”¢×ĘÉÕ”¢³ĘÖŲ | ¹ĢĢåYµÄÖŹĮæĪŖ1.020g |
| ¢Ū | Ļņ²½Öč¢ŚĖłµĆµÄĀĖŅŗÖŠµĪ¼ÓĒāŃõ»ÆÄĘČÜŅŗ£¬µ÷½ŚpHÖĮ12£¬¹żĀĖ”¢Ļ“µÓ”¢×ĘÉÕ”¢³ĘÖŲ | ¹ĢĢåZµÄÖŹĮæĪŖ1.200g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żŃõ»ÆÄĘ¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į | |
| B£® | 3Ħ¶ū¹żŃõ»ÆÄĘ·¢Éś·“Ó¦£¬ÓŠ12Ħ¶ūµē×Ó×ŖŅĘ | |
| C£® | ŌŚøßĢśĖįÄĘÖŠĢśĪŖ+4¼Ū£¬¾ßÓŠĒæŃõ»ÆŠŌ£¬ÄÜĻū¶¾É±¾ś | |
| D£® | øßĢśĖįÄĘ¼ČŹĒŃõ»Æ²śĪļÓÖŹĒ»¹Ō²śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
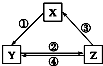 ²»ÄÜŹµĻÖČēĶ¼ĖłŹ¾µÄ±ä»ÆµÄŹĒ£Ø””””£©
²»ÄÜŹµĻÖČēĶ¼ĖłŹ¾µÄ±ä»ÆµÄŹĒ£Ø””””£© | Ń”Ļī | X | Y | Z | ¼żĶ·ÉĻĖł±źŹż×ֵķ“Ó¦Ģõ¼ž |
| A | CaO | Ca£ØOH£©2 | CaCO3 | ¢Ł³£ĪĀÓöĖ® |
| B | AlCl3 | NaAlO2 | Al£ØOH£©3 | ¢ŚĶØČėCO2 |
| C | Na2CO3 | NaOH | NaHCO3 | ¢Ü¹żĮæCa£ØOH£©2ČÜŅŗ |
| D | Cl2 | Ca£ØClO£©2 | HClO | ¢Ū¼ÓÅØŃĪĖį |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
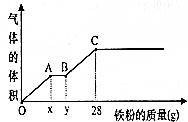 ½«400mLĻ”ĮņĖįŗĶĻ”ĻõĖįµÄ»ģŗĻČÜŅŗĘ½·Ö³ÉĮ½·Ż£®ĻņĘäÖŠŅ»·ŻÖŠÖš½„¼ÓČėĶ·Ū£¬×ī¶ąÄÜČܽā19.2gĶ£¬ĒŅ·“Ó¦ŗóČÜŅŗÖŠ»¹ÓŠĮņĖįŹ£Óą£»ĻņĮķŅ»·ŻÖŠÖš½„¼ÓČėĢś·Ū£¬²śÉśĘųĢåµÄĢå»żŗĶĖł¼ÓĢś·ŪÖŹĮæµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£Ø¼ŁÉčĻõĖįÖ»±»»¹ŌĪŖNOĘųĢ壩£ŗ
½«400mLĻ”ĮņĖįŗĶĻ”ĻõĖįµÄ»ģŗĻČÜŅŗĘ½·Ö³ÉĮ½·Ż£®ĻņĘäÖŠŅ»·ŻÖŠÖš½„¼ÓČėĶ·Ū£¬×ī¶ąÄÜČܽā19.2gĶ£¬ĒŅ·“Ó¦ŗóČÜŅŗÖŠ»¹ÓŠĮņĖįŹ£Óą£»ĻņĮķŅ»·ŻÖŠÖš½„¼ÓČėĢś·Ū£¬²śÉśĘųĢåµÄĢå»żŗĶĖł¼ÓĢś·ŪÖŹĮæµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£Ø¼ŁÉčĻõĖįÖ»±»»¹ŌĪŖNOĘųĢ壩£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 26£ŗ9 | B£® | 39£ŗ9 | C£® | 40£ŗ9 | D£® | 53£ŗ9 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0 |
| ¶ž | ¢Ł | ¢Ś | ||||||
| Čż | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | ||
| ĖÄ | ¢į | ¢ā |
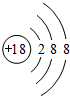
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | sp2ŌӻƹģµĄŠĪ³É¦Ņ¼ü”¢Ī“ŌӻƵÄ2p¹ģµĄŠĪ³É¦Š¼ü | |
| B£® | sp2ŌӻƹģµĄŠĪ³É¦Š¼ü”¢Ī“ŌӻƵÄ2p¹ģµĄŠĪ³É¦Ņ¼ü | |
| C£® | C”¢HÖ®¼äŠĪ³ÉµÄŹĒs-p ¦Ņ¼ü£¬C”¢CÖ®¼äµÄ¦Š¼üŹĒĪ“²Ī¼ÓŌӻƵÄ2p¹ģµĄŠĪ³ÉµÄ | |
| D£® | C”¢CÖ®¼äŠĪ³ÉµÄŹĒsp2-sp2¦Ņ¼ü£¬C”¢HÖ®¼äŹĒĪ“²Ī¼ÓŌӻƵÄ2p¹ģµĄŠĪ³ÉµÄ¦Š¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
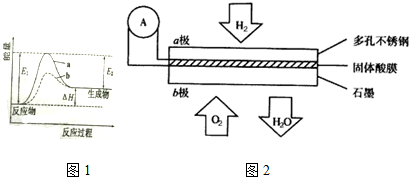
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com