
| A. | 0.1mol Na2O2与足量CO2反应转移的电子的物质的量为0.1mol | |
| B. | 将Na2O2粉末加入到饱和NaOH溶液中,OH-离子浓度一定不变 | |
| C. | 等物质的量的Na2O2与Na2O溶于等质量水中得到的NaOH的物质的量浓度相同 | |
| D. | 等质量的Na2O2与Na2S晶体中含有相同数目的阴离子 |
分析 A、过氧化钠与水和二氧化碳的反应是自身的氧化还原反应;
B、随着一小块Na2O2固体的投入,氢氧化钠饱和溶液中水被反应所消耗,饱和溶液析出固体溶质;由于溶液温度不变,变化后所得溶液仍为氢氧化钠的饱和溶液;
C、Na2O和Na2O2物质的量相等且由方程式易知,Na2O2放在溶液中增加的质量为Na2O2中的Na2O部分,由此可知两溶液的质量相同;
D、Na2O2与Na2S的摩尔质量相等,而且过氧化钠中含有阳离子与阴离子的数目之比为2:1.
解答 解:A、过氧化钠与水和二氧化碳的反应是自身的氧化还原反应,所以0.1mol Na2O2与足量CO2反应转移的电子的物质的量为0.1mol,故A正确;
B、随着一小块Na2O2固体的投入,氢氧化钠饱和溶液中水被反应所消耗,饱和溶液析出固体溶质;由于溶液温度不变,变化后所得溶液仍为氢氧化钠的饱和溶液,如果温度不变,氢氧根离子浓度不变,故B错误;
C、Na2O和Na2O2物质的量相等且由方程式易知,Na2O2放在溶液中增加的质量为Na2O2中的Na2O部分,由此可知两溶液的质量相同,则NaOH的物质的量浓度相同,故C正确;
D、Na2O2与Na2S的摩尔质量相等,而且过氧化钠中含有阳离子与阴离子的数目之比为2:1,所以等质量的Na2O2与Na2S晶体中含有相同数目的阴离子,故D正确;
故选B.
点评 本题考查钠的重要化合物和溶液浓度的计算,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:解答题
| 实验编号 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.40mL |
| 第二次 | 3.00mL | 21.10mL |
| 第三次 | 0.20mL | 20.40mL |
| 第四次 | 0.00mL | 18.20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在测定中和热的实验中,为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 | |
| B. | 酸碱中和滴定实验中,锥形瓶要用待装液预先润洗 | |
| C. | 在测定中和热的实验中,用0.5mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 | |
| D. | 测溶液PH值时,PH试纸不能润湿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当电池负极消耗m g气体时,电解池阴极同时有m g气体生成 | |
| B. | 电池的正极反应式为:O2+2H2O+4e-═4OH- | |
| C. | 电池中c(KOH)不变;电解池中溶液pH变大 | |
| D. | 电解后c(Na2CO3)不变,且溶液中有Na2CO3﹒10H2O晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:10:100:1 | B. | 1:10-1:10-12:10-14 | ||
| C. | 14:13:12:14 | D. | 1:2:12:14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8 g | B. | 11.2 g | C. | 5.6 g | D. | 8.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
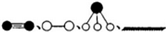 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图1表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图1表示:
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 7 | 9 |
| n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A. | 若起始时向容器中充入0.64 mol C,则达平衡时吸收的热量为0.12a kJ | |
| B. | 恒温,如果压缩容器体积,B的浓度和体积分数均不变 | |
| C. | 若起始时向容器中充入 0.64 mol A 和 0.64 mol B,则达平衡时 n(C)<0.48 mol | |
| D. | 恒温、恒容,向平衡体系中再充入0.32 mol A,再次平衡时,B的转化率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com