
| A. | ①②③④⑤ | B. | ①②③⑤ | C. | ①③④⑤ | D. | ①②③ |
分析 ①相同条件下,碳酸氢钠的溶解度小;
②碳酸氢钠受热易分解;
③Na2CO3水解程度比NaHCO3大;
④碳酸钠与盐酸反应首先转化为碳酸氢钠,而碳酸氢钠直接与盐酸反应生成氯化钠、二氧化碳和水;
⑤等质量的Na2CO3和NaHCO3,NaHCO3物质的量较多,生成二氧化碳多.
解答 解:①Na2CO3和NaHCO3在相同条件下,碳酸氢钠的溶解度小,则在水中的溶解度为:Na2CO3>NaHCO3,故正确;
②碳酸氢钠受热易分解,不稳定,则Na2CO3比NaHCO3热稳定性强,故正确;
③Na2CO3水解程度比NaHCO3大,物质的量浓度相同时,碳酸钠溶液碱性较大,则物质的量浓度相同时,Na2CO3溶液的pH比NaHCO3溶液的大,故正确;
④碳酸钠与盐酸反应首先转化为碳酸氢钠,而碳酸氢钠直接与盐酸反应生成氯化钠、二氧化碳和水,所以碳酸氢钠比碳酸钠与盐酸反应更剧烈,故错误;
⑤等质量的Na2CO3和NaHCO3,NaHCO3物质的量较多,生成二氧化碳多,故正确;
故选B.
点评 熟记碳酸钠和碳酸氢钠的性质差异是解决问题的关键,注意知识的积累和灵活应用,难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 单位时间内生成nmol A2,同时生成2n mol AB | |
| B. | 反应混合气体总压强不随时间而变化 | |
| C. | 反应混合气体密度不随时间而变化 | |
| D. | 容器中各组分的质量分数不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子或分子 | 要求 |
| A | K+、SO42-、Cl-、HS- | c(K+)<c(SO42-) |
| B | Na+、Al3+、Cl-、SO42- | 滴加氨水立即有沉淀产生 |
| C | NH4+、Ba2+、NO3-、CH3COOH | 滴加NaOH溶液立即有气泡产生 |
| D | Fe3+ Na+、NO3-、ClO- | 溶液pH=l |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②④⑥ | C. | ②③④⑤ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向水中滴入少量稀盐酸,平衡逆向移动,Kw减小 | |
| B. | 将水加热,Kw增大,pH减小 | |
| C. | 向水中加入少量固体CH3COONa固体,平衡逆向移动,c(H+)降低 | |
| D. | 向水中加入少量固体硫酸钠,c(H+)和Kw均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
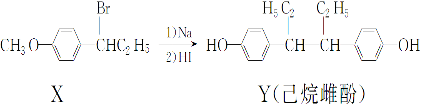
| A. | 在NaOH 水溶液中加热,化合物X 可发生消去反应 | |
| B. | 在一定条件下,化合物Y可与浓溴水发生取代反应 | |
| C. | 用FeCl3溶液不能鉴别化合物X和Y | |
| D. | 化合物Y中不含有手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(SO42-)=c(HS-)=c(K+)>c(OH-)=c(H+) | |
| B. | c(Na+)>c(K+)>c(S2-)>c(H+)>c(OH-) | |
| C. | c(Na+)=c(S2-)+c(HS-)+c(H2S)+c(SO42-) | |
| D. | c(K+)+c(Na+)+c(H+)=c(SO42-)+c(S2-)+c(HS-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
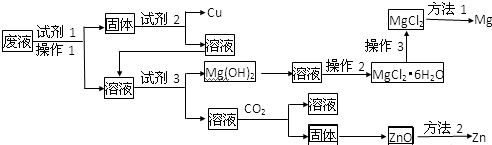
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2g氧气所含氧分子数为0.2NA | |
| B. | 1L0.1mol/L NaCl 溶液中所含的Na+为0.1NA | |
| C. | 0.012 kg 12C中含有碳原子数约为NA | |
| D. | 24g镁变成镁离子时失去的电子数为2N A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com