
【题目】Ⅰ.向体积为2 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:2X(g)![]() Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为____________,X的转化率为__________,Z的平衡浓度为_______________。
Y(g)+3Z(g)。经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的化学反应速率为____________,X的转化率为__________,Z的平衡浓度为_______________。
Ⅱ.一定温度下,反应N2(g)+O2(g)![]() 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
(1)缩小体积使压强增大:__________;
(2)恒容充入N2:__________;
(3)恒容充入He:__________;
(4)恒压充入He:__________。
【答案】0.03mol/(L·min) 20% 0.45mol/L 增大 增大 不变 减小
【解析】
Ⅰ.根据三段式计算;
Ⅱ.根据外界条件对化学反应速率的影响分析。
Ⅰ.向体积为2L的固定密闭容器中通入3mol X气体,在一定温度下发生如下反应:2X(g)![]() Y(g)+3Z(g),经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,气体压强之比等于气体物质的量之比,设生成Y物质的量为x,则
Y(g)+3Z(g),经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,气体压强之比等于气体物质的量之比,设生成Y物质的量为x,则
2X(g)![]() Y(g)+3Z(g)
Y(g)+3Z(g)
起始量(mol) 3 0 0
变化量(mol) 2x x 3x
平衡量(mol)3-2x x 3x
(3+2x)/3=1.2 ,解得x=0.3mol,用Y表示的化学反应速率v(Y)=△c/△t=0.3mol÷(2L×5min)=0.03mol/(L·min);
X转化率=消耗量/起始量×100%=2×0.3mol/3mol×100%=20%;
Z的平衡浓度为c(Z)=n/V=0.3mol×3/2L=0.45mol·L-1;
Ⅱ.(1)缩小体积使压强增大:相当于增大反应物的浓度,化学反应速率增大;
(2)恒容充入N2:增大反应物的浓度,化学反应速率增大;
(3)恒容充入He:不改变反应物的浓度,化学反应速率不变;
(4)恒压充入He:相当于扩大容器的体积,反应物的浓度降低,化学反应速率减小。


科目:高中化学 来源: 题型:
【题目】已知单质铜与稀硝酸的反应为3Cu+8HNO3===2NO↑+4H2O+3Cu(NO3)2(Cu的相对原子质量为64)。现把19.2 g Cu放入200 mL 5 mol·L-1硝酸中,充分反应,问:
(1)哪种物质过量?______
(2)参加反应的硝酸的物质的量为多少?______
(3)在标准状况下产生的气体的体积为多少?______
(4)生成水的分子数为多少?______
(5)若反应前后溶液的体积不变,则生成Cu(NO3)2的物质的量浓度为多少?______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含原子个数比为__,分子的物质的量之比为__。
(2)等温、等压下,等体积的O2和O3所含分子个数比为__,质量比为___。
(3)设NA为阿伏加德罗常数的数值,如果ag氧气中含有的分子数为b,则cg氧气在标准状况下的体积约是___(用含NA的式子表示)。
(4)常温下,将20g质量分数为14%的KNO3溶液跟30g质量分数为24%的KNO3溶液混合,得到密度为1.15g·cm-3的混合溶液。该混合溶液的物质的量浓度为___mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
A. ①④⑥B. ①②④C. ②③⑤D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化钌是一种重要的贵金属化合物,广泛应用于氯碱工业中金属阳极钌涂层及加氢催化剂。
I.三氯化钌的制备
将金属钌粉与氯化钠混合后,加入微量还原性淀粉,将温度升高到800~1000°C,再往熔融的熔体中通入氯气,大部分钌粉转化为氯钌酸钠(Na2RuCl6),再经过一系列化学工艺制备出三氯化钌。
(1)生成氯钌酸钠的化学方程式为__________________
(2)升温阶段加入还原性淀粉的作用是__________________
II.三氯化钌的回收
从废弃催化剂回收三氯化钌的一种工艺流程如下图所示:
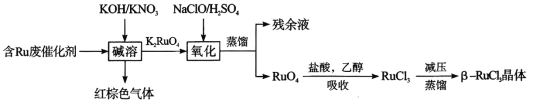
回答下列问题:
(3)“氧化”时加H2SO4的目的______________________
(4)“吸收”过程中加入乙醇的作用是__________________________
(5)可用氢还原重量法测定产品的纯度,其原理为2RuCl3+3H2==2Ru+6HCl。某同学对产品纯度进行测定,所得数据记录如下:

则产品的纯度为________(用百分数表示,保留两位有效数字)
(6)钌及其化合物在合成工业.上有广泛用途,下图是用钌( Ru)基催化剂催化合成甲酸的过程。每生成92g液态HCOOH放出62.4kJ的热量。
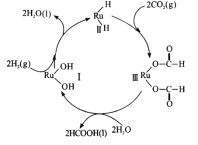
①根据图示写出该反应的热化学方程式_______________
②下列说法正确的是________
a.图示中物质I为该反应的催化剂
b.图示中参与循环的物质只有CO2和H2
c.反应的活化能为62.4 kJ·mol -1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在某密闭容器中进行如下反应:
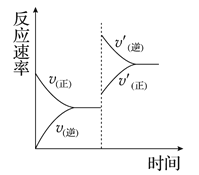
mA(g)+nB(g)![]() pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )
A. 正反应是吸热反应 B. 逆反应是放热反应
C. m+n<p+q D. m+n>p+q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,密闭容器中发生反应4A(s)+3B(g) ![]() 2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1,对此反应速率的表示正确的是( )
2C(g)+D(g),经2 min B的浓度减少0.6 mol·L-1,对此反应速率的表示正确的是( )
A. 用A表示的反应速率是0.4 mol·L-1·min-1
B. 2 min末的反应速率v(C)=0.3 mol·L-1·min-1
C. 2 min内D的物质的量增加0.2mol
D. 若起始时A、B的物质的量之比为4:3,则2 min末A、B的转化率之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当电解质中某离子的浓度越大时,其氧化性或还原性越强。利用这一性质,有人设计出如图所示“浓差电池”(其电动势取决于物质的浓度差,是由一种物质从高浓度向低浓度转移而产生的)。实验开始先断开K1,闭合K2,发现电流计指针发生偏转。下列说法错误的是
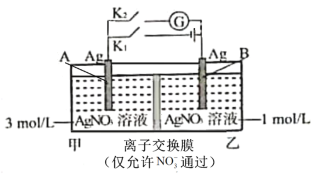
A.断开K1、闭合K2,一段时间后电流计指针归零,此时两池Ag+浓度相等
B.断开K1、闭合K2,当转移0.1mol e-时,乙池溶液质量增加17.0 g
C.当电流计指针归零后,断开K2、闭合K1,一段时间后B电极的质量增加
D.当电流计指针归零后,断开K2、闭合K1,乙池溶液浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3 mL浓硫酸,再加入2 mL乙酸,充分摇匀。在右试管中加入5 mL饱和Na2CO3溶液。按图连接好装置,用酒精灯对左试管小火加热3~5 min后,改用大火加热,当观察到右试管中有明显现象时停止实验。

(1)写出左试管中主要反应的化学方程式:_________________________________。
(2)加入浓硫酸的作用:_________________。
(3)反应开始时用酒精灯对左试管小火加热的原因是____________________________(已知乙酸乙酯的沸点为77 ℃;乙醇的沸点为78.5 ℃;乙酸的沸点为117.9 ℃);后改用大火加热的目的是______。
(4)分离右试管中所得乙酸乙酯和饱和Na2CO3溶液的操作为________(只填名称),所需主要仪器为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com