
中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,a、b、c、d均为Pt电极。
下列说法正确的是
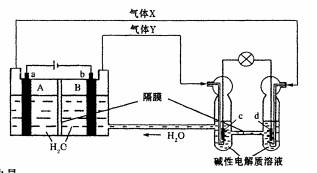
A、B区的OH-通过隔膜向a电极移动,A区pH增大
B、图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应
C、c是正极,电极上的电极反应为: 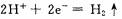
D、当有1mol电子转移时,b电极产生气体Y的体积为11.2L
科目:高中化学 来源: 题型:
有三个烧杯,分别盛有氯化铜、氯化钾和硝酸银三种溶液,均以Pt作电极,将它们串联在一起电解一定时间,测得电极增重总和为2.8 g,这时产生的有色气体与无色气体的物质的量之比为( )
A.4∶1 B.1∶1 C.4∶3 D.3∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
冶炼铜矿石所获得的铜通常含有锌、铁、镍、银、金和铂等微量杂质,俗称粗铜。工业上通常通过电解法除去这些杂质制得精铜,以提高铜的使用价值,扩大铜的应用范围。(几种金属的相对原子质量是:Fe-56,Ni-59,Cu-64,Zn-65,Ag-108,Au-197。)
请完成下列问题:
(1)一般来说,电解精炼铜的初始电解质溶液里的阳离子是__________,写出铜的电解精炼过程中的阴极反应式________________________________。
(2)如果转移0.020 mol e-,下列说法中一定正确的是________。
①阴极质量增加0.64 g ②阳极质量减少0.64 g
③电解质溶液的质量保持不变 ④电解质溶液的温度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
橡胶属于重要的工业原料。它是一种有机高分子化合物,具有良好的弹性,但强度较差。为了增强某些橡胶制品的强度,加工时往往需硫化处理,即将橡胶原料与硫黄在一定条件下反应。橡胶制品硫化程度越高,强度越大,弹性越差。下列橡胶制品中,加工时硫化程度较高的是 ( ) 。
。
A.橡皮筋 B.汽车外胎
C.普通气球 D.医用乳胶手套
查看答案和解析>>
科目:高中化学 来源: 题型:
对于结构满足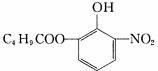 的有机物,下列瞄述中正确的是
的有机物,下列瞄述中正确的是
A、分子中有2种含氧官能团 B、能发生取代、加成、消去、氧化反应
C、1mol该有机物最多消耗3mol NaOH D、苯环上的一溴代物最多有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(DGa与B同主族,Ga的基态原子核外电子排布式为
第一电离能由大到小的顺序是
(2)硼酸(H3B03)是白色片状晶体(层状结构如右图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
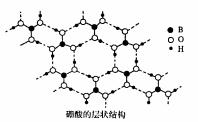
①硼酸中B原子的杂化轨道类型为 。
②硼酸晶体中存在的作用力有范德华力和 。
③加热时,硼酸的溶解度增大,主要原因是 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OHˉ 而呈酸性。写出硼酸的电离方程式_ 。
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理 。 [BH4]-的空问构型是____。
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式 。
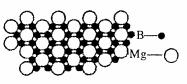
(5)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,右图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为 。
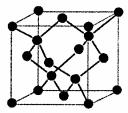
(6)金刚石的晶胞如右图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5pm,则立方氮化硼的密度是____g· cmˉ 3
(只要求列算式,不必计算出数值,阿伏伽德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气(含有烃类、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂钯合金作催化剂)。它的特点是使CO和NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)下列说法错误的是 。
A.CO和NOx反应的化学方程式为2xCO+2NOx 2xCO2+N2
2xCO2+N2
B.上述方法的缺点是由于CO2增多,会大大提高空气的酸度
C.多植树造林,增大绿化面积,可有效控制城市空气各种污染源
D.汽车改用天然气为燃料或开发氢能源,都会减少对空气的污染
(2)写出CO与NO反应的化学方程式_____________________。
(3)“催化转换器”的缺点是在一定程度上提高了空气的酸度,其原因是___________________________________________。
(4)控制城市空气污染源的方法可以有 (填序号)。
A.开发氢能源 B.使用电动车
C.植树造林 D.戴上呼吸面具
( 5)汽车尾气可引起光化学烟雾,主要是 气体。形成酸雨主要是 气体,在尾气转化中,主要还会产生 气体,造成温室效应。
5)汽车尾气可引起光化学烟雾,主要是 气体。形成酸雨主要是 气体,在尾气转化中,主要还会产生 气体,造成温室效应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com