
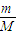 计算铜的物质的量,根据n=cV计算NO3-、H+的物质的量,根据反应3Cu+2NO3-+8H+=3Cu2++2NO+4H2O进行过量计算,根据不足量的物质计算n(Cu2+),再根据c=
计算铜的物质的量,根据n=cV计算NO3-、H+的物质的量,根据反应3Cu+2NO3-+8H+=3Cu2++2NO+4H2O进行过量计算,根据不足量的物质计算n(Cu2+),再根据c=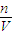 计算;
计算;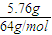 =0.09mol,
=0.09mol, n(H+)=
n(H+)= ×0.08mol=0.03mol,
×0.08mol=0.03mol,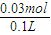 =0.3 mol/L
=0.3 mol/L n(Cu)=
n(Cu)= ×0.09mol=0.06mol,故原溶液中n(HNO3)=n(NO3-)=0.06mol.需要n(H+)=
×0.09mol=0.06mol,故原溶液中n(HNO3)=n(NO3-)=0.06mol.需要n(H+)= n(Cu)=
n(Cu)= ×0.09mol=0.24mol,根据电荷守恒可知n(H+)=n(NO3-)+2n(SO42-),即0.24mol=0.06mol+2n(SO42-),解得n(SO42-)=0.09mol,故n(H2SO4)=n(SO42-)=0.09 mol,
×0.09mol=0.24mol,根据电荷守恒可知n(H+)=n(NO3-)+2n(SO42-),即0.24mol=0.06mol+2n(SO42-),解得n(SO42-)=0.09mol,故n(H2SO4)=n(SO42-)=0.09 mol,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2011?杭州一模)氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行:
(2011?杭州一模)氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2011?郑州二模)利用所学化学反应原理,解决以下问题:
(2011?郑州二模)利用所学化学反应原理,解决以下问题:| H | + 4 |
| H | + 4 |
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol H2、1mol I2 | 2 mol HI | 4 mol HI |
| HI的浓度(mol?L-1) | C1 | C2 | C3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 反应物转化率 | a1 | a2 | a3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com