
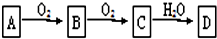
| ||
| 1 |
| 2 |


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、⑤②①③⑥ |
| B、①②③④⑤⑦ |
| C、⑤②①③⑧ |
| D、①②⑤③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
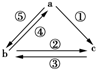 如图所示各步转化关系中,①②③反应是化合反应,④⑤反应是置换反应,则表中各物质之间不能通过一步反应实现如图所示转化关系的是( )
如图所示各步转化关系中,①②③反应是化合反应,④⑤反应是置换反应,则表中各物质之间不能通过一步反应实现如图所示转化关系的是( )| 物质 选项 | a | b | c |
| A | C | CO2 | CO |
| B | Br2 | FeBr2 | FeBr3 |
| C | Al | AlCl3 | Al2O3 |
| D | Fe | FeCl2 | FeCl3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、IBr可与水反应生成HIO和HBr |
| B、在高温下用氢气还原MgCl2可制取金属镁 |
| C、Na久置于空气中,最终生成NaHCO3 |
| D、打开盛浓盐酸的试剂瓶可看到白色的雾,说明HCl不稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生如下反应:
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生如下反应:| A、反应方程式中的x=1 |
| B、t1~t3间该反应的平衡常数均为4 |
| C、t3时刻改变的条件是移去少量物质D |
| D、t3时刻改变的条件是使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1 NaHB溶液 pH=4,则溶液中:c(HB-)>c(B2-)>c(H2B) |
| B、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:c(NH4+)+c(Fe2+)=0.3 mol?L-1 |
| C、NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| D、Na2CO3溶液中:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Na+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com