
| 2MQ |
| m |
| 2MQ |
| m |
| 2MQ |
| m |


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
A、 25℃时,向亚硫酸溶液中通入氯气 |
B、 向NaAlO2溶液中通入HCl气体 |
C、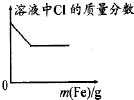 向少量氯化铁溶液中加入铁粉 |
D、 向BaSO4饱和溶液中加入硫酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150mL 1mol?L-1的NaCl |
| B、25mL 2mol?L-1的FeCl3 |
| C、150mL 3mol?L-1的KCl |
| D、75mL 2mol?L-1的CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C4H8可能是烯烃 |
| B、C4H8中属于烯烃类的同分异构体有4种 |
C、核磁共振氢谱有2种吸收峰的烯烃结构一定是  |
| D、C4H8中属于烯烃的顺反异构体有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③⑤ | B、①②④⑤⑥ |
| C、①②③④⑤ | D、全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com