
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶
液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有__________________________________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是___________________________;
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________;
(4)要加快上述实验中气体产生的速率,还可采取的措施有___________________(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液 分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=__________,V6=__________,V9=________。
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色;
③该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因。
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
实验室制备下列气体时,所用方法正确的是( )
A.制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置
B.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体
C.制乙烯时,用排水法或向上排空气法收集气体
D.制二氧化氮时,用水或NaOH溶液吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是: (用离子方程式表示)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为 (填代号)。
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
(2)由滤液B制备少量无水AlCl3(AlCl3极易在空气中水解)
①由滤液B制备氯化铝晶体(将AlCl3•6H2O)涉及的操作为: 、冷却结晶、 (填操作名称)、洗涤。
②将AlCl3•6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的 (填序号).
①氧化性 ②吸水性 ③难挥发性 ④脱水性
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号)。
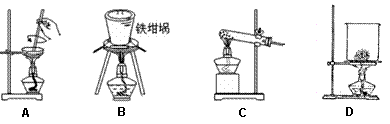
查看答案和解析>>
科目:高中化学 来源: 题型:
分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )
①液体量不超过烧瓶容积,不少于.
②温度计的水银球应位于蒸馏烧瓶支管口附近.
③为防止暴沸,应在烧瓶中加入沸石或碎瓷片.
④冷凝管中冷却水下进上出,先加热,再通水.
⑤按各组分沸点控制分馏温度,并收集在同一锥形瓶中
⑥停止加热后,应继续通水冷却冷凝管中蒸气.
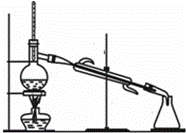
|
| A. | ①③④ | B. | ②③④ | C. | ③④⑤ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上从废铅蓄电池的铅膏回收铅的过程中,可用碳酸盐溶液与处理后的铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO (aq)PbCO3(s)+SO
(aq)PbCO3(s)+SO (aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(1)上述反应的平衡常数表达式:K=____________________________________。
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,在________溶液中PbSO 4转化率较大,理由是___________________________。
4转化率较大,理由是___________________________。
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3·Pb(OH)2],它和PbCO3受热都易分解生成PbO。该课题组对固体产物(不考虑PbSO4)的成分提出如下假设,请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二:_____________________________________________________________;
假设三:____________________________________ _________________________。
_________________________。
(4)为验证假设一是否成立,课题组进行如下研究。
①定性研究:请你完成下表中内容。
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取一定量样品充分干燥,…… |
②定量研究:取26.7 mg的干燥样品,加热,测得固体质量随温度的变化关系如下图:

某同学由图中信息得出结论:假设一不成立。你是否同意该同学的结论,并简述理由:
__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机化合物A的相对分子质量大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。下列叙述不正确的是( )
A.该化合物分子中含有4个氧原子
B.该化合物的相对分子质量是134
C.该化合物的化学式(分子式)是C5H10O4
D.该化合物分子中最多含2个 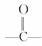 官能团
官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽 草酸的说法正确的是
草酸的说法正确的是
 A.分子式为C7H6O5
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaOH反应的有( )
①—OH ②—CH3 ③—COOH ④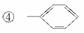 ⑤—CHO
⑤—CHO
A.2种 B.3种
C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类生活密切相关。关于下列物质的使用不合理的是
A.单质硅可用于制造光纤制品 B.碳酸氢钠常用于焙制糕点
C.氧化铝可用于制造耐火坩埚 D.氢氧化铝常用于治疗胃酸过多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com