
A、H2O2: |
B、HClO: |
C、MgCl2: |
D、CCl4 |
 ,故A错误;
,故A错误;  ,故B错误;
,故B错误; ,故C正确;
,故C正确;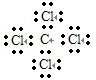 ,故D错误.
,故D错误.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、C2H5OH |
| B、CrO3 |
| C、H2SO4 |
| D、Cr2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NA个Fe原子的质量为56g,则1个Fe原子的质量为
| ||
B、20℃时,铝的密度为2.7g?cm-3,则1个Al原子的体积为
| ||
C、4℃时,水的密度为1.0g?cm-3,则1个H2O分子的体积为
| ||
D、标准状况下,NA个N2分子所占的体积约为22.4L,则1个N2分子的体积为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①②④ |
| C、①②③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向溶液Fe(NO3)2中加入少量稀氢碘酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
| B、Ba(OH)2溶液中加入过量的Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
| C、将足量的CO2通入Ca(ClO)2溶液中:2ClO-+CO2+H2O═2HClO+CO32- |
| D、向酸性KMnO4溶液中滴加双氧水:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有光学活性,发生下列反应后生成的有机物无光学活性的是( )
有光学活性,发生下列反应后生成的有机物无光学活性的是( )| A、与甲酸发生酯化反应 |
| B、与NaOH水溶液共热 |
| C、与银氨溶液作用 |
| D、在催化剂存在下与HCN作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将40gNaOH溶解于1L水中配成的NaOH溶液 |
| B、从1000mL1mol/L NaCl溶液中取出100mL的溶液 |
| C、将1L10mol/L的浓盐酸与9L水混合而成的溶液 |
| D、常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B、常温常压下,22.4LCO2中含有的CO2分子数小于NA个 |
| C、等物质的量的N2和CO的质量均为28g |
| D、常温下,1L 0.1mol/LNa2CO3溶液中,含有阴离子的总数小于0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com