
| A. | 原子化热由大到小:Na>Mg>Al | |
| B. | 晶格能由大到小:NaF>NaCl>NaBr>NaI | |
| C. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| D. | 晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
分析 A、原子化热是用来衡量金属键强弱的物理量,指将1摩尔金属转变成气态原子所需的最小能量;金属原子化热数值小时,其熔点低,质地软,反之则熔点高,硬度小;
B、晶格能与离子半径成反比,与电荷成正比;
C、原子晶体中化学键键能越大、键长越短其硬度越大;
D、分子晶体,相对分子质量越大,分子间作用力越大,熔点越高.
解答 解:A、根据金属镁、铝和钠的熔点可知,金属的原子化热最大的为铝,其次为镁,最小的为钠,正确关系为:Al>Mg>Na,故A错误;
B、晶格能与离子半径成反比,与电荷成正比,离子半径,F-<Cl-<Br-<I-,则晶格能NaF>NaCl>NaBr>NaI,故B正确;
C、原子晶体中化学键键能越大、键长越短其硬度越大,这几种物质都是原子晶体,键长C-C<C-Si<Si-Si,所以硬度:金刚石>碳化硅>晶体硅,故C正确;
D、四种分子晶体的组成和结构相似,分子的相对分子质量越大,分子间作用力越大,则晶体的熔沸点越高,故D正确;
故选A.
点评 本题考查晶体熔沸点高低判断,侧重考查晶体类型判断及晶体熔沸点高低影响因素,注意晶格能、金属键与离子半径、离子所带电荷关系,题目难度不大.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:解答题
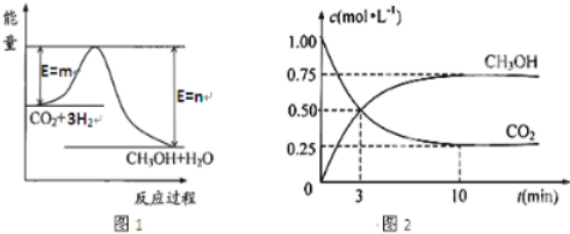
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |
| 2 | 4 | 1.6 | 2.4 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 长江三角洲的形成 | |
| B. | 雾天容易看到车灯形成的光柱 | |
| C. | 将植物油倒入水中用力搅拌形成油水混合物 | |
| D. | 向氢氧化铁胶体中加入硫酸溶液先出现浑浊后变澄清 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③ | C. | ①④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ③⑤ | C. | ①③④ | D. | ①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com