
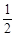 O2 (g)
O2 (g) | A.– 283.01 kJ · mol – 1 | B.+ 172.51 kJ · mol –1 |
| C.+ 283.01 kJ · mol – 1 | D.+ 504.00 kJ · mol – 1 |
科目:高中化学 来源:不详 题型:填空题
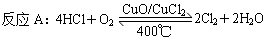
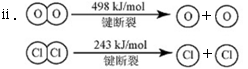
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.N2(g)+3H2(g)===2NH3(l) ΔH=2(a-b-c)kJ·mol- |
| B.N2(g)+3H2(g)===2NH3(g) ΔH=2(b-a)kJ·mol-1 |
| C.1/2 N2 (g)+3/2H2(g)===NH3(l) ΔH=(b+c-a)kJ·mol-1 |
| D.1/2 N2(g)+3/2H2(g)===NH3(g) ΔH=(a+b)kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g) +
2NH3(g) + 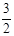 O2(g) ;△H =" a" kJ·mol—1
O2(g) ;△H =" a" kJ·mol—1| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
 2NH3(g) ΔH= -92.4kJ·mol—1
2NH3(g) ΔH= -92.4kJ·mol—1 2H2O(l) ΔH = -571.6kJ·mol—1
2H2O(l) ΔH = -571.6kJ·mol—1查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.奥运火炬燃烧时的能量转化主要是由化学能转变为热能 |
| B.相同条件下,正丁烷的热值比丙烷大 |
| C.正丁烷比异丁烷不稳定 |
| D.异丁烷分子中的碳氢键比正丁烷的多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a>b>c | B.a>c>b | C.c>b>a | D.b>a>c |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 =2H2O(g) △H2=-483.6 kJ·
=2H2O(g) △H2=-483.6 kJ·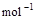
| A.+131.3kJ·mol—1 | B.-131.3kJ·mol—1 |
| C.+373.1kJ·mol—1 | D.-373.1kJ·mol—1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com