
【题目】下列物质中含有离子键的是
A.H2B.MgCl2C.HClD.CO2
科目:高中化学 来源: 题型:
【题目】汽车尾气中通常含有NxOy和CO等大气污染物,科学家寻找高效催化剂实现了汽车尾气的转化进而减少汽车尾气对大气的污染。
(1)己知:①CO的燃烧热△H1=-283kJ·mol-1 ②N2(g)+O2(g) =2NO(g) △H2 =+183kJ·mol-1
由此写出NO和CO反应的热化学反应方程式________________________________。
(2)一定温度下,向2L密闭容器中充入4.0mo1NO2和4.0molCO,在催化剂作用下发生反应 4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H<0,测得相关数据如下:
N2(g)+4CO2(g) △H<0,测得相关数据如下:
0 min | 5 min | 10 min | 15 min | 20 min | |
c(NO2)/ mol·L-1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
C(N2)/ mol·L-1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①5l0min,用N2的浓度变化表示的反应速率为__________________。
②以下表述能说明该反应己达到平衡状态的是________。
A.气体颜色不再变化 B.气体密度不再变化 C.气体平均相对分子质量不再变化
③20 min时,保持温度不变,继续向容器中加入1.0mol NO2和1.0molCO,在t1时刻反应再次达到平衡,则NO2的转化率比原平衡 ______________(填“增大”、“减小”或“不变)。
④该温度下反应的化学平衡常数K= __________ (保留两位有效数字)。
(3)CO、空气与过量KOH溶液可构成燃料电池(石墨为电极):
①写出该电池的负极反应式____________________________;
②常温下,用该燃料电池电解(惰性电极)1L饱和食盐水(足量),当两极共生成4.48L (折算为标准状况)气体时电解池溶液的pH=__________。(忽略溶液的体积变化,己知1g2=0.3,lg5=0.7)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 在0.01mol·L-1Ba(OH)2溶液中:Al3+、NH4+、NO![]() 、HCO
、HCO![]()
B. 0.1mol/L的FeCl2溶液中:H+、Al3+、SO42-、ClO-
C. 滴加KSCN溶液显红色的溶液:NH4+、K+、Cl-、I-
D. 由水电离产生的c(H+)=1×10-13mol·L-1的溶液中:Na+、Ba2+、NO![]() 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生活、社会可持续发展密切相关,下列说法正确的是( )
A. 地球上最基本的能源是化学能
B. 太阳能热水器、沼气的使用、玉米制乙醇都涉及生物质能的利用
C. 利用二氧化碳制造全降解塑料能有效减少“白色污染”
D. 人们可以把放热反应释放的能量转化为其它可利用的能量,而吸热反应没有利用价值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,所含原子数相等的是( )
A.10g H2和10g O2
B.标准状况下相同体积的N2和H2
C.9g水和0.25mol H2
D.22g CO2和3.01×1023个N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示实验中,能够达到目的的是( )
A | B | C | D |
|
|
|
|
制取并收集氨气 | 验证:非金属性Cl>C>Si | 检验浓硫酸与铜反应的产物中是否含铜离子 | 验证铁发生析氢腐蚀 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有多种污染物。一定条件下,通过下列反应可实现汽车尾气的合理排放:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H<0
N2(g)+2CO2(g) △H<0
若反应在恒容的密闭容器中进行,下列说法正确的是( )
A. 随着反应的进行,容器内压强逐渐减小
B. 及时分离出N2或CO2,正反应速率加快
C. 其他条件不变时降低温度,可提髙反应物的转化率
D. 其他条件不变时使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.稀硫酸滴在银片上:2Ag+2H+═2Ag++H2↑
B.硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO ![]() ═BaSO4↓
═BaSO4↓
C.硝酸银溶液与盐酸反应:Ag++Cl﹣═AgCl↓
D.澄清石灰水与碳酸钠溶液反应:Ca(OH)2+CO ![]() ═CaCO3↓+2OH﹣
═CaCO3↓+2OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾(K2Cr2O7)主要用于制革、印染、电镀等。其水溶液中存在平衡:![]() +H2O
+H2O![]() 2
2![]() +2H+
+2H+
(1)已知有关物质溶解度如图1。用复分解法制备K2Cr2O7的操作过程是:向Na2Cr2O7溶液中加入_________(填化学式),搅拌溶解,调节溶液pH约为5,加热溶液至表面有少量晶体析出时,_____________,抽滤得到粗产品,再用重结晶法提纯粗产品。
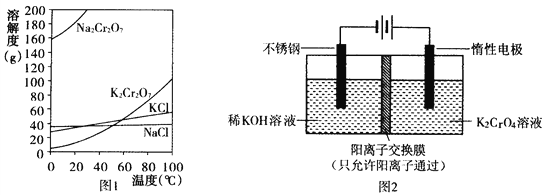
(2)以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图2。
①不锈钢作________极,写出该电极的电极反应式________________________。
②分析阳极区能得到重铬酸钾溶液的原因________________________。
③当铬酸钾的转化率达到x时,阳极液中K与Cr的物质的量之比为____________。
(3)铬对环境能造成污染。某酸性废水中含有![]() ,处理时可用焦亚硫酸钠(Na2S2O5)将
,处理时可用焦亚硫酸钠(Na2S2O5)将![]() 转化为毒性较低的Cr3+,再调节pH约为8,使铬元素沉降,分离出污泥后检测废水中Cr3+浓度,低于0.5mg·L-1则达到排放标准。
转化为毒性较低的Cr3+,再调节pH约为8,使铬元素沉降,分离出污泥后检测废水中Cr3+浓度,低于0.5mg·L-1则达到排放标准。
①Na2S2O5参加反应的离子方程式为____________________。
②经上述工艺处理后的废水,理论上Cr3+浓度约为__________mg·L-1。(已知室温下Ksp≈6×10-31)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com