
| A. | 8.5 | B. | 17 | C. | 16 | D. | 34 |
分析 令A的物质的量为2mol,由方程式可知,若A完全分解混合气体总物质的量为4mol,根据混合气体相对氢气密度计算混合气体的相对分子质量;若A完全不反应,根据m=nM计算混合气体总质量,由质量守恒定律可知A的质量等于混合气体总质量,再根据M=$\frac{m}{n}$计算A的相对分子质量,则A的相对分子质量介于上述两极值之间.
解答 解:令A的物质的量为2mol,
若A完全反应,由方程式2A=B+3C,可知混合气体总物质的量为1mol+3mol=4mol,混合气体对氢气的相对密度为4.25,则混合气体平均相对分子质量=2×4.25=8.5,
若A完全不反应,混合气体总质量=4mol×8.5g/mol=34g,由质量守恒定律可知A的质量为34g,则A的相对分子质量为$\frac{34}{2}$=17,
故A的相对分子质量介于8.5~17之间,
故选:C.
点评 本题考查混合物计算,注意利用极限法解答,关键是确定极限法的两个端点,为易错题目,学生容易忽略可逆反应而错选B.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 用浓硝酸可以鉴别毛织物和棉织物 | |
| B. | 葡萄糖和蔗糖不是同分异构体,但是同系物 | |
| C. | 羊毛完全燃烧只生成CO2和H2O | |
| D. | 某学生设计了如图实验方案用以检验淀粉水解的情况: 由以上实验可以得出淀粉已完全水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCO3、MgO、Mg2N3 | B. | MgCO3、MgO、Mg(OH)2 | C. | MgO、Mg2N3、C | D. | MgCO3、C、Mg2N3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g | B. | 50g | C. | 72g | D. | 80g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
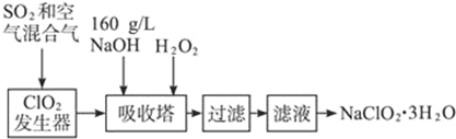
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
| 相对式量 | 112.5 | 147 | 162.5 | 128 |
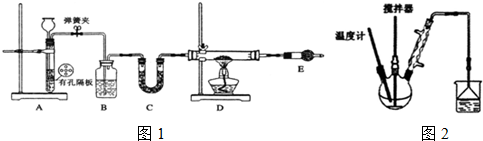
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.2 NA | |
| B. | 标准状况下,5.6L水中含有的分子数为0.25NA | |
| C. | 20g D2O中含有的质子数目为10NA | |
| D. | 标准状况下,22.4 LCO2和O2混合气体中含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
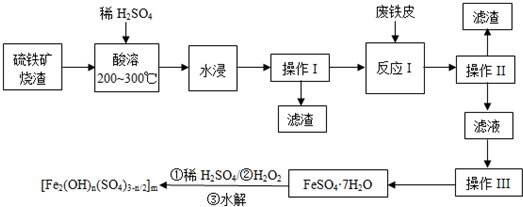
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com