
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g)![]() 2SO3(g);ΔH =-196.6kJ/mol,测得反应的相关数据如下:
2SO3(g);ΔH =-196.6kJ/mol,测得反应的相关数据如下:
容器1 | 容器2 | 容器3 | |
反应温度 T/K | 700 | 700 | 800 |
反应物投入量 | 2molSO2、1mol O2 | 4molSO3 | 2molSO2、1mol O2 |
平衡v正(SO2)/ mol·L-1 ·s-1 | v1 | v2 | v3 |
平衡c(SO3)/ mol·L-1 | c1 | c2 | c3 |
物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(O2) |
平衡常数K | K1 | K2 | K3 |
下列说法正确的是 ( )
A.v1<v2,c2<2c1B.K1>K3 ,p2>2p3
C.v1<v
【答案】D
【解析】
对比容器的特点,将容器1和容器2对比,将容器1和容器3对比。容器2中加入4molSO3等效于在相同条件下反应物投入量为4molSO2、2molO2,容器2中起始反应物物质的量为容器1的2倍,容器2相当于在容器1达到平衡后增大压强,将容器的体积缩小到原来的一半,增大压强反应速率加快,则v1>v2,增大压强平衡向正反应方向移动,平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO2)<1;容器1和容器2的温度相同,则K1=K2;容器3相当于在容器1达到平衡后升高温度,升高温度反应速率加快,则v1<v3,升高温度平衡逆向移动,平衡时c3<c1,p3>p1,α1(SO2)>α3(SO2),K1>K3,据此分析解答。
容器2中加入4molSO3等效于在相同条件下反应物投入量为4molSO2、2molO2,容器2中起始反应物物质的量为容器1的2倍,容器2相当于在容器1达到平衡后增大压强,将容器的体积缩小到原来的一半,增大压强反应速率加快,则v1<v2,增大压强平衡向正反应方向移动,平衡时c2>2c1,p2<2p1,α1(SO2)+α2(SO2)<1;容器1和容器2的温度相同,则K1=K2;容器3相当于在容器1达到平衡后升高温度,升高温度反应速率加快,则v1<v3,升高温度平衡逆向移动,平衡时c3<c1,p3>p1,α1(SO2)>α3(SO2),K1>K3。
A.根据分析可知,v1<v2,c2>2c1,故A错误;
B.K1>K3,p2<2p1,p3>p1,则p2<2p3,故B错误;
C.根据分析可知:v1<v3,α1(SO2)>α3(SO2),故C错误;
D.c2>2c1,c3<c1,则c2>2c3;α1(SO2)+α2(SO2)<1,α1(SO2)>α3(SO2),则α2(SO3)+α3(SO2)<1,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
(1)将一定量的有机物A置于氧气中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该有机物的实验式是__。
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图1所示的质谱图,则其相对分子质量为___,该物质的分子式是__。
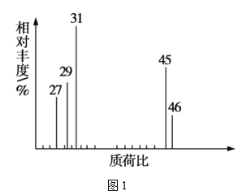
(3)根据价键理论,预测A的可能结构并写出结构简式:___。
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的吸收峰(信号),根据吸收峰(信号)可以确定分子中氢原子的种类和数目。例如氯甲基甲基醚(Cl-CH2-O-CH3,有2种氢原子)的核磁共振氢谱如图2所示:

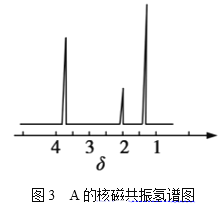
经测定,有机物A的核磁共振氢谱图如图3所示,则A的结构简式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量。下列叙述正确的是( )

A.F表示反应生成Cu的物质的量
B.E表示反应实际消耗H2O的物质的量
C.E表示反应生成O2的物质的量
D.F表示反应生成H2SO4的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种芳香族化合物A,其蒸气密度是相同条件下H2密度的82倍,A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为73.2%和7.32%。
(1)A的分子式是__;
(2)已知:
ⅰ.![]() (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
ⅱ.![]()
又知,A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去.

请回答:
①步骤Ⅰ的目的是__;
②若G为气体,且相对分子质量是44,则E的结构简式是__;E的核磁共振氢谱中有__个吸收峰(填数字);
③F→H的反应类型是__;
④F在一定条件下可发生酯化反应,生成M(M与FeCl3反应,溶液呈紫色;且分子结构中含有苯环和一个七元环)请写出该反应的化学方程式__;
⑤A的结构简式是__;
上述转化中B→D的化学方程式是__;
(3)已知A的某种同分异构体K具有如下性质:
①K与FeCl3反应,溶液呈紫色
②K在一定条件下可发生银镜反应
③K分子中苯环上的取代基上无甲基
请写出K所有可能的结构简式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列性质比较结果错误的是( )
A.碳碳键键长:乙烯>苯B.沸点:正戊烷>异戊烷
C.相对密度: ![]() >
> ![]() D.水溶性:CH3CH2OH>CH3CH2Br
D.水溶性:CH3CH2OH>CH3CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着环保意识增强,清洁能源越来越受到人们关注。
(1)甲烷是一种理想的洁净燃料。已知:CH4(g)+2O2(g)= CO2(g)+ 2H2O(g);△H= -802.3kJ·mol-1 H2O(1)=H2O(g),△H =+44.0kJ·mol-l
写出常温常压下甲烷完全燃烧的热化学方程式____,计算4.8g甲烷气体完全燃烧生成液态水,放出热量为____kJ。
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值。该反应为CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H=+206.lkJ·mol-l。
CO(g)+3H2(g)△H=+206.lkJ·mol-l。
①800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表。
CH4 | H2O | CO | H2 |
3.0 molL1 | 8.5 molL1 | 2.0 molL1 | 2.0 molL1 |
则此时正、逆反应速率的关系是正反应速率____逆反应速率。(填“>”、“<”、“=”)
②为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。
实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/ molL1 | H2O初始浓度/ molL1 |
1 | 360 | p | 2.00 | 6.80 |
2 | t | 101 | 2.00 | 6.80 |
3 | 360 | 101 | 2.00 | 6.80 |
表中t=___,P=____;设计实验2、3的目的是____;实验l、2、3中反应的化学平衡常数的大小关系是____(用K1、K2、K3表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(![]() ),发生反应:
),发生反应:![]()
![]()
![]() ,体系中c(Pb2+)和c(Sn2)变化关系如右图所示。下列判断正确的是
,体系中c(Pb2+)和c(Sn2)变化关系如右图所示。下列判断正确的是
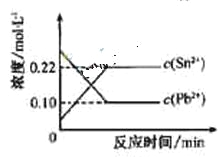
A.往平衡体系中加入少量金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量![]() 固体后,c(Sn2-)变小
固体后,c(Sn2-)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应![]()
D.25℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四组物质,用横线上所给的试剂常温下就能鉴别出来的是( )
A.FeO、FeS、CuO、CuS、稀硫酸
B.苯、四氯化碳、无水乙醇、己烯 溴水
C.甲酸、乙酸、乙醛、乙醇 新制氢氧化铜悬浊液
D.苯酚钠溶液、甲苯、乙酸乙酯、乙酸 饱和碳酸钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com