
| A.除去石英中混有的少量铝粉,可加入氢氧化钠溶液溶解后过滤 |
| B.向含有少量的FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液,以除去FeC12溶液中的FeBr2 |
| C.除去乙酸乙酯中混有的少量乙酸,加入饱和氢氧化钠溶液振荡后分液 |
| D.巳知:Ksp (CuS)<Ksp (FeS),可加入过量的难溶电解质FeS,使水中少量的Cu2+转化成硫化物沉淀而除去 |
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源:不详 题型:单选题
 Fe2+ + Ag+。下列铁盐中洗涤效果最好的是
Fe2+ + Ag+。下列铁盐中洗涤效果最好的是| A.FeCl3 | B.Fe2(SO4)3 | C.Fe2(CO3)3 | D.FeCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验序号 | 实验 | 实验现象 | 结论 |
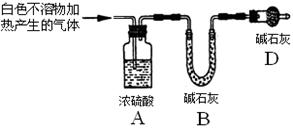
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成分为___?___ |
| 实验Ⅲ | 取实验I中的白色不溶物,洗涤,加入足量 ? | ? | 白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验I中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在 ④ 离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
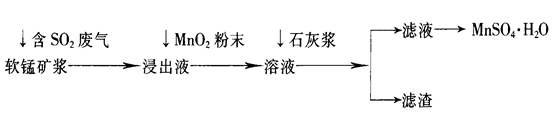
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
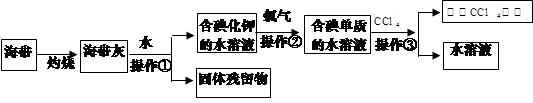
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
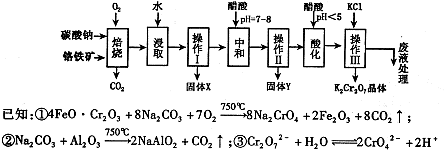

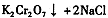 。该反应在溶液中能发生的理由是: 。
。该反应在溶液中能发生的理由是: 。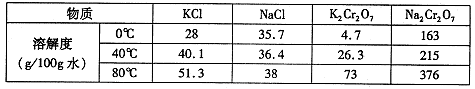
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用乙醇萃取碘水中的碘 |
| B.用饱和NaHCO3溶液除去CO2中的HCl |
| C.用Ba(NO3)2溶液鉴别SO32-和SO42- |
| D.用淀粉KI溶液鉴别FeCl3溶液和溴水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
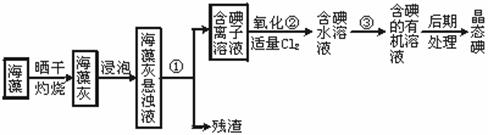
| A.乙酸 | B.苯 | C.四氯化碳 | D.酒精 |
| 有机试剂 | 酒精 | 四氯化碳 | 苯 | 乙酸 |
| 毒性 | 无 | 无 | 有 | 无 |
| 水溶性 | 与水以任意比互溶 | 与水互不相溶 | 与水互不相溶 | 与水以任意比互溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com