
下列说法正确的是( )
A.原子最外层电子数大于3(小于8)的元素一定是非金属元素
B.原子最外层只有1个电子的元素一定是金属元素
C.最外层电子数比次外层电子数多的元素一定位于第2周期
D.某元素的离子的最外层与次外层电子数相同,该元素一定位于第3周期
科目:高中化学 来源: 题型:
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出(已知硝酸的还原产物是NH4NO3)。在反应结束后的溶液中,逐滴加入5mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量关系如下图所示。则
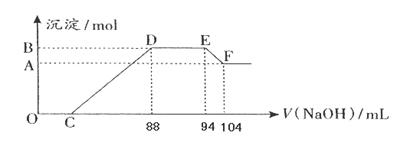
(1)B与A的差值为: mol
(2)原硝酸溶液中含硝酸的物质的量为: mol。
(3)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为:
(4)写出铝与该浓度硝酸反应的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,②是工业上重要的反应之一。

请回答下列问题:
(1)H的电子式是________________,其中含有的化学键类型是___________
_________________。
(2)写出反应④的现象:_______________________________________________________________________________________,
有关反应的化学方程式为_______________________________________________________________________。
(3)已知I的燃烧热是-285.8 kJ·mol-1,则1 m3(标准状况)I完全燃烧,恢复至室温时放出的热量是________(计算结果保留3位有效数字)。
(4)25 ℃时,以Pt为电极电解含有少 量酚酞的F的饱和溶液,则在________(填“阴”或“阳”)极附近溶液由无色变为红色,若在此极收集到0.2 g气体,则此时溶液的pH是________(假设溶液的体积为2 L且不考虑电解后溶液体积的变化)。
量酚酞的F的饱和溶液,则在________(填“阴”或“阳”)极附近溶液由无色变为红色,若在此极收集到0.2 g气体,则此时溶液的pH是________(假设溶液的体积为2 L且不考虑电解后溶液体积的变化)。
(5)在K溶液中加入与K等物质的量的Na2O2,恰好使K转化为N,写出该反应的离子方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式:
__________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为__________,其水溶液与F单质反应的化学方程式为____________________________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显______色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成 具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为__________。
具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是( )
A.IA族与VIIA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,水解程度越大
D.同周期金属元素的化合价越高,其原子失电子能力越强
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家从化肥厂生产的(NH4)2SO4中检验出组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO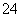 和N2H
和N2H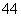 两种离子形式存在,植物的根系极易吸收N4H
两种离子形式存在,植物的根系极易吸收N4H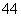 ,但它遇到碱时,会生成一种形似白磷的N4分子。N4分子 不能被植物吸收。下列有关说法不正确的是( )
,但它遇到碱时,会生成一种形似白磷的N4分子。N4分子 不能被植物吸收。下列有关说法不正确的是( )
A.N4和N2互为同素异形体
B.14N与14C互为同位素
C.N4H4(SO4)2不能与草木灰混合使用
D.8NH3+4C5OH===N4+4C5NH2+6H2+4H2O,此反应中每生成5.6 g N4时转移1.2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素的叙述正确的是( )
A.金属元素与非金属元素能形成共价化合物
B.只有在原子中,质子数才与核外电子数相等
C.目前使用的元素周期表中,最长的周期含有36种元素
D.由非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,Y为单质,当X无论是强酸还是强碱时,都有如下的转化关系:
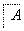
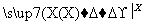
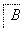
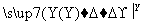
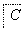
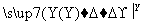
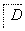
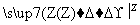

当X是强酸时,A、B、C、D、E均含有同一种元素,当X是强碱时,A、B、C、D、E均含有另外同一种元素。请回答:
(1)A是________,Y是________,Z是________。
(2)当X是强酸时,E是________,写出B生成C的化学方程式:_______________ _________________________________________________________。
(3)当X是强碱时,E是________,写出B生成C的化学方程式:_______________ _________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源。已知制酒精的方法有三种:
①在催化剂作用下乙烯与水反应;
②CH3CH2Br+H2O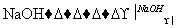 CH3CH2OH+HBr;
CH3CH2OH+HBr;
③(C6H10O5)n(淀粉)+nH2O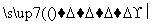 nC6H12O6(葡萄糖);
nC6H12O6(葡萄糖);
C6H12O6(葡萄糖)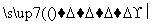 2C2H5OH+2CO2↑。
2C2H5OH+2CO2↑。
(1)方法①的化学方程式是________________________________________。
(2)方法②的化学反应类型是____________。
(3)为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?请简述理由
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是________。
A.① B.③
C.①③ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com