
【题目】镁、铝、铁合金投入300mL ![]() 溶液中,金属恰好溶解,分别转化成
溶液中,金属恰好溶解,分别转化成![]() 和
和![]() ;还原产物为NO,在标准状况下体积为6.72L。在反应后的溶液中加入300mL某浓度的NaOH溶液,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g。下列有关推断正确的是( )
;还原产物为NO,在标准状况下体积为6.72L。在反应后的溶液中加入300mL某浓度的NaOH溶液,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g。下列有关推断正确的是( )
A.参加反应的![]() 的物质的量为0.9molB.NaOH的物质的量浓度为6
的物质的量为0.9molB.NaOH的物质的量浓度为6![]()
C.参加反应的金属的质量为11.9gD.![]() 的物质的量浓度为3
的物质的量浓度为3![]()
【答案】C
【解析】
镁、铝、铁合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Mg2+离子,根据电子得失守恒、原子守恒计算。
将镁、铝、铁合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Mg2+离子,根据电子守恒,金属共失去电子的物质的量为:![]() =0.9mol,反应中金属失去电子的物质的量=生成物硝酸盐中硝酸根离子的物质的量=生成碱中的氢氧根离子的物质的量,即:n(OH-)=n(NO3-)=0.9mol,则
=0.9mol,反应中金属失去电子的物质的量=生成物硝酸盐中硝酸根离子的物质的量=生成碱中的氢氧根离子的物质的量,即:n(OH-)=n(NO3-)=0.9mol,则
A.参加反应的硝酸的物质的量为:n(HNO3)=n(NO3-)+n(NO)=0.3mol+0.9mol=1.2mol,A选项错误;
B.沉淀达到最大量时,溶液中的溶质为硝酸钠,由钠离子守恒可知,氢氧化钠溶液的物质的量浓度为:c(NaOH)=![]() =3mol/L,B选项错误;
=3mol/L,B选项错误;
C.反应后沉淀的质量=金属质量+m(OH-)=金属质量+0.9mol×17g/mol=27.2g,则金属的质量为:27.2g-15.3g=11.9g,C选项正确;
D.参加反应的硝酸的物质的量为:n(HNO3)=n(NO3-)+n(NO)=0.3mol+0.9mol=1.2mol,硝酸的物质的量浓度为:c(HNO3)= ![]() =4mol/L,D选项错误;
=4mol/L,D选项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是( )
![]()
A.原子半径Q>R>T
B.原子序数比R多1的元素只能形成一种氢化物
C.W原子得电子能力强于Q原子,且可形成共价化合物QW2
D.与W同一主族的下一周期元素不可作为半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: +4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O。可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点为9.79℃、131.4℃,不溶于水);试管d中装有适量液溴(表面覆盖少量水)。
+4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O。可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点为9.79℃、131.4℃,不溶于水);试管d中装有适量液溴(表面覆盖少量水)。

(1)e装置的作用是_______________;当观察到______________________________现象时,试管d中反应基本结束。
(2)若用冰水代替烧杯中的冷水,可能引起的不安全后果是_________________________。
(3)实验结束后精制试管d中粗产品,操作先后顺序是___________________。
A.蒸馏 B.水洗 C.用干燥剂干燥 D.10%NaOH溶液洗
(4)实验消耗40%乙烯利溶液50g,制得产品mg,则乙烯利合成1,2-二溴乙烷的产率为________________(列出含m的计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列图像的分析正确的是
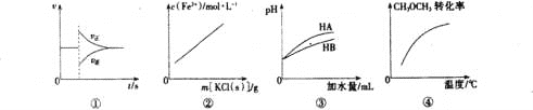
A. 图①可表示反N2(g)+3H2(g) ![]() 2NH3(g)在达到平衡后,臧少NH3的浓度,正逆反应速率的变化趋势
2NH3(g)在达到平衡后,臧少NH3的浓度,正逆反应速率的变化趋势
B. 图②表示FeCl3溶液和KSCN溶液反应达平衡后,向该混合液中逐渐加人固体KCl的过程中C(Fe3+)的变化趋势(忽略溶液体积变化)
C. 图③表示等体积等pH的弱酸HA和强酸HB加水稀释过程中的pH变化趋势
D. 图④表示密闭容器中CH3OCH3(g)+3H2O(g) ![]() 6H2(g)+2CO2(g) △H>0达到平衡后,恒压升高温度过程中,CH3OCH3的转化率变化趋势
6H2(g)+2CO2(g) △H>0达到平衡后,恒压升高温度过程中,CH3OCH3的转化率变化趋势
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,11.2 L四氯化碳中含有的分子数0.5NA
B.常温常压下,18.0 g水所含的电子数为10 NA
C.300mL 0.1mol/L的NaCl的溶液含有0.03NA个NaCl分子
D.1.2 g熔融的NaHSO4含有阴阳离子总数为0.03NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生态农业涉及农家废料的综合利用,某种肥料经发酵得到一种含甲烷、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有足量红热CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO![]() CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过足量的澄清石灰水,充分吸收生成沉淀8.5 g。下列说法正确的是
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过足量的澄清石灰水,充分吸收生成沉淀8.5 g。下列说法正确的是
A.硬质玻璃管中固体减少的氧元素的物质的量为0.15mol
B.原混合气体中甲烷的物质的量是0.75mol
C.原混合气体中氮气的体积分数为5.56%
D.原混合气体中二氧化碳的物质的量为0.085mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把7.5 g镁铝合金的粉末放入200ml 4mol/L的盐酸中,往充分反应后的混合溶液中逐渐滴入一定物质的量浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如图所示。

(1)合金中镁的物质的量为_______。
(2)氢氧化钠的物质的量浓度为_______mol/L。
(3)V1=_______mL。
(4)写出该合金溶于足量NaOH溶液的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2的一些性质或用途如图,下列说法正确的是( )

A. ①、②、③三个反应中MnO2均作氧化剂
B. 足量MnO2与2 L 10 mol/L HCl共热,可生成5 mol Cl2
C. 反应②若生成1 mol Al2O3,则反应过程中转移12 mol电子
D. 反应③中K2CO3和KNO3的化学计量数均为1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是25℃时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | 1.8×10-10 | 2.0×10-12 | 1.8×10-5 | 3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.碳酸钠溶液中滴加少量氯水的离子方程式H2O+CO32-+Cl2=HCO3-+Cl-+HClO
C.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COO-):c(CH3COOH)=9:5,此时溶液pH=5
D.向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol·L-1的AgNO3,CrO42-先沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com