

| ||
| ||
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
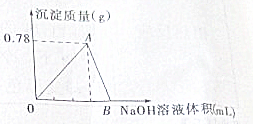 向20mL AlCl3溶液中滴入2mol?L-1 NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示:
向20mL AlCl3溶液中滴入2mol?L-1 NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
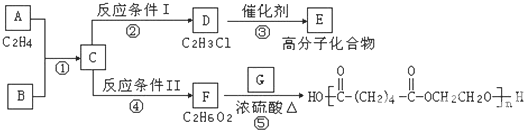
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 有关问题 |
| (1)计算所需KCl的质量 | 需要KCl的质量为 |
| (2)称量KCl固体 | 称量过程中主要用到的仪器是 |
| (3)将KCl溶解在100mL烧杯中 | 为加速溶解,可采取的措施是 |
| (4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应采取的措施是 |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某种胃药的止酸剂为碳酸钙,测定每片中碳酸钙含量的方法有以下几步操作(设药片中的其他成分不与盐酸或氢氧化钠反应):
某种胃药的止酸剂为碳酸钙,测定每片中碳酸钙含量的方法有以下几步操作(设药片中的其他成分不与盐酸或氢氧化钠反应):| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V/mL | 12.9 | 15.4 | 13.1 | 13.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
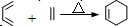
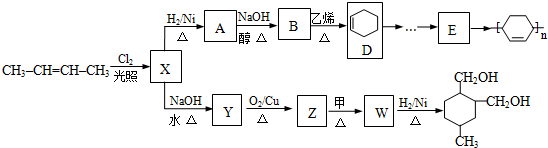
| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
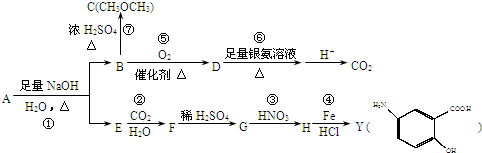

| Fe |
| HCl |
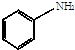
 和
和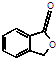 ,鉴别I和J的试剂为
,鉴别I和J的试剂为 )制得.请写出以L为原料制得M的合成路线流程图(无机试剂任用).流程图示例如下:
)制得.请写出以L为原料制得M的合成路线流程图(无机试剂任用).流程图示例如下:| HBr |
| NaOH溶液 |
| △ |
 )→
)→查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂白精的有效成分是Ca(ClO)2 |
| B、利用高纯硅的半导体性能,可以制成光电池 |
| C、NO、NO2是大气污染物,能在空气中稳定存在 |
| D、HCl、NH3、BaSO4都是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com