
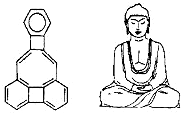
 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),有关该有机分子的说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),有关该有机分子的说法正确的是( )| A. | 该有机物属于烃的衍生物 | B. | 该有机物属于苯的同系物 | ||
| C. | 该有机物分子中含有22个碳原子 | D. | 该有机物一氯代物只有4种 |
分析 A.该物质中只含C、H元素;
B.苯的同系物含有1个苯环,侧链为烷基;
C.键线式中交点、端点为C原子,结合有机物结构的交点判断C原子数目;
D.根据等效氢进行判断.
解答 解:A.该物质中只含C、H元素,所以属于烃而不是烃的衍生物,故A正确;
B.苯的同系物含有1个苯环,侧链为烷基,该烃不是苯的同系物,故B错误;
C.该有机物结构简式中交点为碳原子,分子中含有22个碳原子,12个H原子,故C正确;
D.该有机物分子为左右对称,分子中含有6种化学环境不同的H原子,其一氯代物有6种,故D错误;
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查基本概念、物质结构判断等知识点,易错选项是D,注意等效氢的判断方法,题目难度不大.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | X、Y两元素最简单氢化物的稳定性:X<Y | |
| B. | Z、W的氧化物均能与稀硫酸反应 | |
| C. | Z和W的氧化物均可作耐高温材料 | |
| D. | W的单质可用于制备光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
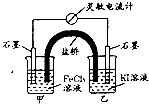 控制合适的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法不正确的是( )
控制合适的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法不正确的是( )| A. | 盐桥中的K+移向FeCl3溶液 | |
| B. | 反应开始时,乙中石墨电极上发生氧化反应 | |
| C. | 电流计读数为零时,反应达到化学平衡状态 | |
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电级为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

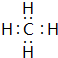 .稳定性最强的结构式为
.稳定性最强的结构式为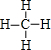 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子和氯离子都属于氯元素 | |
| B. | 合金中一定含有金属元素 | |
| C. | 人体缺铁元素会引起贫血 | |
| D. | 碳和碘元素都是人体不可缺少的微量元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
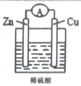
| A. | 每当Zn片质量减少65克,Cu片会产生22.4L气体 | |
| B. | 溶液的pH逐渐减小 | |
| C. | 电子从锌片经导线流向铜片 | |
| D. | 氢离子在铜片表面被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
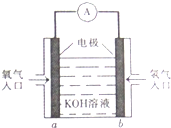 被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从a、b两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从a、b两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
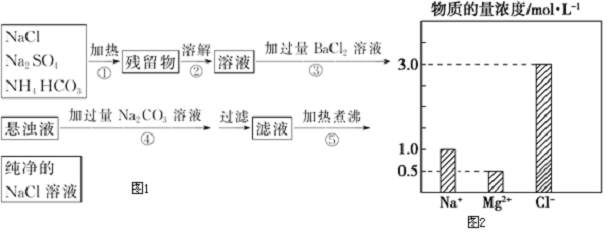
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com