
����Ŀ��������к͵ζ��ķ����ⶨNaOH��Na2CO3�Ļ��Һ�е�NaOH����ʱ�������ڻ��Һ�мӹ�����BaCl2��Һ��ʹNa2CO3��ȫ���BaCO3������Ȼ���ñ�����ζ����÷�̪��ָʾ�����������й�ʵ���˵����ȷ���ǣ� ��
A.�����BaCO3������NaOH��Һ�е������ᣬ����Ӱ��NaOH�����IJⶨ
B.�ζ�ʱ�����ζ����еζ�Һһֱ�½����������Ŵﵽ�ζ��յ㣬��Ӱ�������
C.���ü�����ָʾ������ⶨ���ƫС
D.���Բ��ý�Na2CO3��ȫ���BaCO3������ֱ�ӵμӱ����ᣬ�����������ݲ���
���𰸡�A
���������⣺A����̪�ı�ɫ��Χ��8��10����ʱBaCO3���ܽ⣬��Һ��������䣬��Ӱ��NaOH�����IJⶨ����A��ȷ��
B�����ݵζ��ܵ��¶��̶ȣ����ζ�Һһֱ�½������������������Һ�������NaOH�������ⶨ����B����
C�����ȵı�ɫ��Χ��3.1��4.4����ʱBaCO3�ܽ⣬��Һ�����ƫ����c�����⣩= ![]() ��֪���ⶨ���ƫ��C����
��֪���ⶨ���ƫ��C����
D��ֱ�ӵμӱ����ᣬ�����������ݲ�����̼�����������ᷴӦ����Һ�����ƫ����c�����⣩= ![]() ��֪���ⶨ���ƫ��D����
��֪���ⶨ���ƫ��D����
��ѡ��A��
�����㾫����������Ҫ����������к͵ζ������֪ʶ�㣬��Ҫ�����к͵ζ�ʵ��ʱ��������ˮϴ���ĵζ������ñ�Һ��ϴ����װ��Һ�����ô���Һ��ϴ������ȡҺ�壻�ζ��ܶ���ʱ�ȵ�һ�����Ӻ��ٶ������۲���ƿ����Һ��ɫ�ĸı�ʱ���ȵȰ������ɫ�����Ϊ�ζ��յ������ȷ�����⣮


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ͬ����ϰ����ʦ����ѧ������ϵ�д�
ͬ����ϰ����ʦ����ѧ������ϵ�д� ����ϰ�⽭��ϵ�д�
����ϰ�⽭��ϵ�д� ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��Ȳ����ڵ����Ҳ�����ڷǵ���ʵ��ǣ� ��
A. NaOHB. C2H5OHC. ʳ��ˮD. CaCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NO2�Ǵ�����Ⱦ��֮һ��ʵ��������NO2��Cl2�����NaOH��Һ���յķ�����������Ⱦ���ش��������⣺
��1���������Ʊ� 
������M��N������������ ��
������MnO2��Ũ�����Ʊ����ռ�һƿ���������������ѡ��ͼ1�е�װ�ã�������˳��Ϊ��������������Сд��ĸ��ʾ����
��D���Ʊ�װ���е��������������ӷ���ʽ��ʾװ��F�������� ��
��2������ͼ2��ʾװ��̽��Cl2��NO2��NaOH��Һ�еķ�Ӧ�� �����й����Ͽ�֪��HNO3��һ�����ᣬ�Ҳ��ȶ����ֽ�����NO��NO2 ��
��װ����X��Z��������
��ʵ��ʱ�۲쵽X�Լ�ƿ���л���ɫ���壬Z�Լ�ƿ���к���ɫ���壬��ͨ���ʵ�������Cl2��NO2 �� Y�й۲첻��������ɫ����Ӧ���������ϡ������������Y�з�����Ӧ�Ļ�ѧ����ʽ�� ��
�۷�Ӧ������ȡY����Һ�������Թ��У�����ϡ���ᣬ���к���ɫ������������Ͳ����������ԭ�� �� 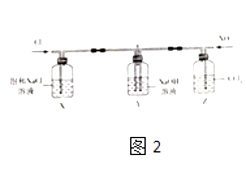
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������ڸ���������һ���ܴ���������ǣ� ��
A.�μӼ����Ժ�ɫ����Һ�У�Na+��K+��Cl����ClO��
B.����KSCN��Ѫ��ɫ����Һ�У�Na+��Mg2+��SO42����Br��
C.![]() =1.0��1012mol/L����Һ�У�K+��Na+��NO3����HCO3��
=1.0��1012mol/L����Һ�У�K+��Na+��NO3����HCO3��
D.��ˮ�����c��H+��=1.0��10��13mol/L����Һ�У�NH4+��Fe2+��NO3����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���a mol/L��ˮ����μ������ᣬ������������ȷ���ǣ� ��
A.pH��С
B.![]() ����
����
C.ˮ�ĵ���̶Ȼ������
D.Kw����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������淴Ӧ��ƽ��ı䷴Ӧ��������仯������ȷ���ǣ� �� 
A.��100mL 0.1mol/L������Һ����������ƾ����������ҺpH�ı仯����ͼ
B.��FeCl3��Һ��KSCN��Һ��Ϻ�Ӧ��ƽ�������Һ���������KCl������c��Fe3+���ı仯����ͼ
C.�ܱ������н���N2��g��+3H2��g��2NH3��g����Ӧ�ﵽƽ����ֺ��º�ѹ�����£���ͨ��ϡ������Ar�Ĺ�����H2��ת���ʱ仯����ͼ
D.�ܱ������н���CH3OCH3��g��+3H2O��g��6H2��g��+2CO2��g����H��0�ﵽƽ����ֺ�ѹ�����£��������¶ȹ�����CH3OCH3��ת���ʱ仯����ͼ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������н��з�Ӧ��X��g��+2Y��g��2Z��g����H��0����ͼ����ȷ��ʾ�÷�Ӧ�й��������仯���ɵ��ǣ� ��
A.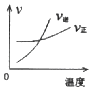
B.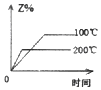
C.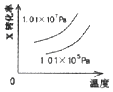
D.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����BaCl2��Һ��ͨ��SO2����Һ��������֧�Թ��У���һ���м���NaOH��Һ�����ְ�ɫ����A����һ��ͨ������Cl2��������ɫ����B���Իش��������⣺
��1����������SO2��ˮ�ķ�Ӧ��BaCl2��Һ��ͨ��SO2������������������������������������Ӧ����Ҳ����������Ӧ�������������˴�ӦΪ ��ԭ���� ��
��2������A�Ļ�ѧʽΪ ���ó����ܷ�����ϡ��� _��
��3��д�����ɳ���B�����ӷ���ʽ�� ��
��4������2.33 g����B�������ı�״���µ�Cl2 mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeS��һ��Ũ�ȵ�HNO3��Ӧ������Fe(NO3)3��Fe2(SO4)3��NO2��NO��H2O����NO2��NO�����ʵ���֮��Ϊ6:1ʱ��ʵ�ʲμӷ�Ӧ��FeS��HNO3�����ʵ���֮��Ϊ
A. 2:11 B. 1:6
C. 1:7 D. 1:8
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com