
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均存在化学键 | |
| C. | 含有金属元素的物质中均存在离子键 | |
| D. | 含有共价键的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 A>B>D>C | |
| B. | 原子序数 d>c>b>a | |
| C. | 离子半径 C>D>B>A | |
| D. | 原子结构的最外层电子数目 A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 少用煤作燃料 | B. | 把工厂烟囱造高 | ||
| C. | 燃烧脱硫煤 | D. | 在已酸化的土壤中加石灰 | ||
| E. | 开发新能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3、NH4NO3 | B. | (NH4)2CO3、NH4NO3 | C. | NH4HCO3、NH4Cl | D. | NH4Cl、(NH4)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

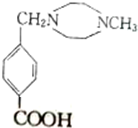 .
.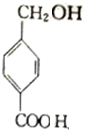 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$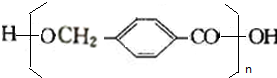 +(n-1)H2O
+(n-1)H2O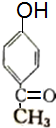 +2Br2→
+2Br2→ +2HBr.
+2HBr.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
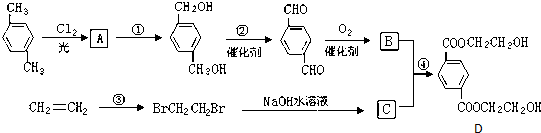
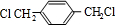 、
、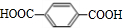 、HOCH2CH2OH.
、HOCH2CH2OH. +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$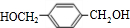 +2NaCl;水解(取代)反应.
+2NaCl;水解(取代)反应.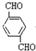 与银氨溶液反应的化学方程式OHCC6H4CHO+4Ag(NH3)2OH$\stackrel{水浴加热}{→}$NH4OOCC6H4COONH4+4Ag↓+6NH3↑+2H2O.
与银氨溶液反应的化学方程式OHCC6H4CHO+4Ag(NH3)2OH$\stackrel{水浴加热}{→}$NH4OOCC6H4COONH4+4Ag↓+6NH3↑+2H2O.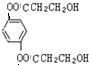 )与足量NaOH溶液反应的化学方程式:
)与足量NaOH溶液反应的化学方程式: +4NaOH→
+4NaOH→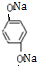 +2HOCH2CHCOONa.
+2HOCH2CHCOONa.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com