
 地球是一个巨大的生态系统,森林对保护改善人类的生存环境有着十分重要的作用.科学实验证明,1公顷柳杉林每月可以吸收SO2160kg,试解答下列问题:
地球是一个巨大的生态系统,森林对保护改善人类的生存环境有着十分重要的作用.科学实验证明,1公顷柳杉林每月可以吸收SO2160kg,试解答下列问题:| 132×20×106 |
| 64 |


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
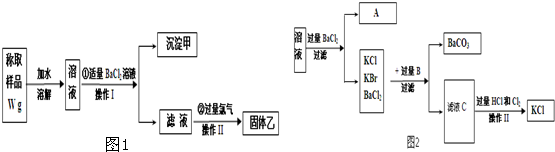
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
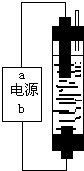 阅读下表中的部分短周期主族元素的相关信息.
阅读下表中的部分短周期主族元素的相关信息.| 元素代号 | 相关信息 |
| T | T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期元素形成的简单离子中,Y的简单离子半径最小 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验序号 | V[Fe2(SO4)3]/mL | V(H2O2)/mL | V(蒸馏水)/mL | 时间t/min | V(氧气)/mL |
| 1 | 1.0 | 10.0 | 5.0 | 2.0 | 10.0 |
| 2 | 2.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2SO4 |
| B、AgNO3 |
| C、NaCl |
| D、AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
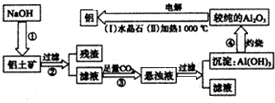

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com