
【题目】下列事实能用勒夏特列原理来解释的是( )
A.SO2氧化SO3,往往需要使用催化剂2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
B.500 ℃左右的温度比室温更有利于合成氮反应N2(g)+ 3H2 (g)![]() 2NH3(g) △H<0
2NH3(g) △H<0
C.H2、I2、HI平衡混合气体加压后颜色加深H2(g)+ I2(g)![]() 2HI(g)
2HI(g)
D.实验室采用排饱和食盐水的方法收集氯气Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A.高压有利于合成氨的反应
B.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
C.红棕色的NO2,加压后颜色先变深后逐渐变浅
D.黄绿色的氯水光照后颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
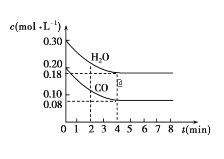
请解答下列各题:
(1)0~4min内的平均反应速率v(CO)=___mol/(L·min),v(H2)=___mol/(L·min),v(CO2)=___mol/(L·min)。
(2)请你在图中标出CO2和H2的浓度变化。___
(3)T℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表。
时间(min) | 0 | 2 | 3 | 4 | 5 | 6 |
CO | 0.200 | 0.138 | c1 | c1 | 0.116 | 0.096 |
H2O | 0.300 | 0.238 | c2 | c2 | 0.216 | 0.266 |
CO2 | 0 | 0.062 | c3 | c3 | 0.084 | 0.104 |
H2 | 0 | 0.062 | c4 | c4 |
①表中3min~4min之间,反应处于___状态;c1___0.08mol/L(填“大于”、“小于”或“等于”)。
②反应在4min~5min之间,平衡向逆反应方向移动,可能的原因是___(单选),表中5min~6min之间数值发生变化,可能的原因是___(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛广泛应用于航天、军事、化工、医疗等领域。钛在高温下易和氧、氮、碳等元素化合,提炼纯钛条件苛刻。从高钛渣![]() 主要为
主要为![]() 提炼海绵钛流程如下:
提炼海绵钛流程如下:
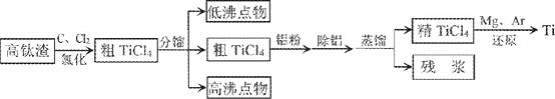
氯化后的粗![]() 中含有
中含有![]() 、
、![]() 、
、![]() 、
、![]() 等杂质,相关物质的沸点如下表:
等杂质,相关物质的沸点如下表:
化合物 |
|
|
|
|
|
沸点 | 136 | 310 |
| 180 | 138 |
回答下列问题:
![]() 高钛渣经过破碎、磁选、磨粉后送氯化车间,磨粉的目的是________。
高钛渣经过破碎、磁选、磨粉后送氯化车间,磨粉的目的是________。
![]() “分馏
“分馏![]() ,原因是________。加入铝粉使
,原因是________。加入铝粉使![]() 转化为
转化为![]() 便于除去,写出铝粉与
便于除去,写出铝粉与![]() 反应的化学方程式:________。
反应的化学方程式:________。
![]() “除铝”的方法是用水湿润的活性炭加入到粗
“除铝”的方法是用水湿润的活性炭加入到粗![]() ,使
,使![]() 转化为________而除去。
转化为________而除去。
![]() “还原”需要在Ar的气氛中进行,原因是________。副产物经电解生成________可循环使用。
“还原”需要在Ar的气氛中进行,原因是________。副产物经电解生成________可循环使用。
![]() 制备钛的一种新型方法是:将
制备钛的一种新型方法是:将![]() 粉末浇注成形,烧结后作阴极,以石墨为阳极,
粉末浇注成形,烧结后作阴极,以石墨为阳极,![]() 为熔盐进行电解
为熔盐进行电解![]() 熔盐不参与电极反应,起溶解和传导
熔盐不参与电极反应,起溶解和传导![]() 的作用
的作用![]() 。
。
![]() 阳极生成的气体除
阳极生成的气体除![]() 外,还有________
外,还有________![]() 填化学式
填化学式![]() 。
。
![]() 阴极的电极反应式为________。
阴极的电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酞菁钴被广泛应用于光电材料、光动力学光敏材料等方面。酞菁钴(II)结构如图所示(Co均形成单键,部分化学键未画明)。下列说法错误的是( )
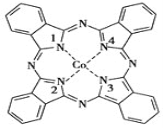
A.酞菁钴(II)中三种非金属元素的电负性大小顺序为N>C>H
B.酞菁钴(II)中碳原子的杂化方式只有sp2杂化
C.1号和3号N原子的VSEPR模型均为平面三角形
D.2号和4号N原子与Co(Ⅱ)是通过配位键结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
A. 550℃时,若充入惰性气体,正,逆 均减小,平衡不移动
B. 650℃时,反应达平衡后CO2的转化率为25.0%
C. T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D. 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数KP=24.0P总
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸钙用途广泛,可用于高硫烟气脱硫助剂,也可作为制备草酸的中间体.据最新文献,氢氧化钙碳基化合成甲酸钙的反应如下:
![]() 反应1
反应1
(1)反应体系中存在以下两个竞争反应
![]() 反应2
反应2
![]() 反应3
反应3
![]() 二氧化碳与氢气直接合成甲酸的热化学反应方程式为 ______ .
二氧化碳与氢气直接合成甲酸的热化学反应方程式为 ______ .
![]() 为了更有利于生成甲酸钙,应选择的反应条件是较低的温度和 ______
为了更有利于生成甲酸钙,应选择的反应条件是较低的温度和 ______ ![]() 填编号
填编号![]() .
.
A.催化剂![]() 低压
低压![]() 高压
高压
(2)如图1是反应2和反应3,lnK与温度T的关系;同一条件时反应2的K ______ ![]() 填“大于”或“小于”
填“大于”或“小于”![]() 反应3的K,这对于 ______
反应3的K,这对于 ______ ![]() 填“反应2”或“反应3”
填“反应2”或“反应3”![]() 不利的.
不利的.
(3)以氢氧化钙初始密度为![]() 、CO的分压为
、CO的分压为![]() 条件下催化反应,以氢氧化钙转化率
条件下催化反应,以氢氧化钙转化率![]() 为坐标,时间为横坐标得到如图2;
为坐标,时间为横坐标得到如图2;

![]() 根据图象选择合适的反应温度 ______ ;理由是 ______ .
根据图象选择合适的反应温度 ______ ;理由是 ______ .
![]() 当
当![]() 为
为![]() 时,产物中甲酸钙与碳酸钙的质量比为50:1,氢氧化钙有 ______
时,产物中甲酸钙与碳酸钙的质量比为50:1,氢氧化钙有 ______ ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式为
A. 用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B. 硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+ Fe2+
C. 向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3![]() =Al2(CO3)3↓
=Al2(CO3)3↓
D. 用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH-=![]() +
+![]() + H2O
+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备(NH4)2Fe(SO4)2·6H2O 的实验中,需对过滤出产品的母液(pH<1)进行处理。室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是
A.通入过量Cl2:Fe2+、H+、![]() 、Cl、
、Cl、![]()
B.加入少量NaClO溶液:![]() 、Fe2+、H+、
、Fe2+、H+、![]() 、ClO
、ClO
C.加入过量NaOH 溶液:Na+、Fe2+、![]() 、
、![]() 、OH
、OH
D.加入过量NaClO和NaOH的混合溶液:Na+、![]() 、Cl、ClO、OH
、Cl、ClO、OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com