
| A、CuS |
| B、Cu(NO3)2 |
| C、Cu(OH)2 |
| D、CuCO3 |
| 1.3×10-36 |
| 3 |
| ||
| 1.4×10-10 |


科目:高中化学 来源: 题型:
| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
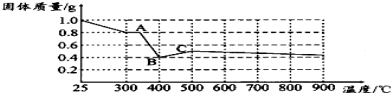
| 取少量黑色固体, |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.27×10-5mol/L |
| B、1.45×10-4mol/L |
| C、2.9×10-4mol/L |
| D、5.8×10-4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HA在水中有0.001%发生电离 |
| B、HA的电离平衡常数K=10-8mol/L |
| C、升高温度时,PH增大 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、恒温,压缩体积,平衡不移动,混合气体颜色加深 |
| B、恒压,充入HI(g),开始时正反应速率减小 |
| C、恒容,升高温度,逆反应速率减小 |
| D、恒容,充入H2,再次达到平衡时H2(g)的体积分数增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com