
| A. | 3.2g | B. | 6.4g | C. | 9.6g | D. | 12.8g |
分析 负极、正极均生成PbSO4附着在电极上,电极质量均增重,铅蓄电池两极的质量差等于电极质量增重之差,由组成差量可知,负极增重为SO42-的质量,而正极增重相当于SO2的质量,结合电子转移守恒计算.
解答 解:负极、正极均生成PbSO4附着在电极上,电极质量均增重,当电路中通过0.4mol电子时,
负极:Pb+SO42--2e-=PbSO4,负极电极增重相当于0.2molSO42-的质量,
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,正极增重相当于0.2molSO2的质量,
故铅蓄电池两极的质量差等于0.2mol×(96g/mol-64g/mol)=6.4g,
故选:B.
点评 本题考查电化学有关计算,侧重考查学生的分析计算能力,注意利用差量法与电子转移守恒进行计算.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧化性酸:HNO3、H3PO4、HClO4 | |
| B. | 干燥剂:碱石灰、硅胶、无水氯化钙 | |
| C. | 酸性氧化物:SiO2、Cl2O、CrO3 | |
| D. | 危险化学品:天然气、金属钠、氯酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
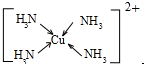 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | |
| B. | CH3COOCH2CH2OOCCH3 乙二酸二乙酯 | |
| C. | CH3CH2CH(OH)CH3 3-丁醇 | |
| D. | 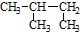 2-甲基丁烷 2-甲基丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 500 | 1000 |
| C(H2O)/mol•L-1 | 5.00 | 3.52 | 2.48 |
| C(CO2)/mol•L-1 | 2.50 |
| A. | 在500s内用H2O(g)表示的化学反应速率是2.96×10-3mol•L-1•s-1 | |
| B. | 在500s时生成的CH4的浓度是0.74mol•L-1 | |
| C. | 在1000s时反应达到平衡 | |
| D. | 0-500s的平均反应速率大于500~1000s的平均反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
物理量 实验序号 | 0.1mol?L-1Fe2(SO4)3 的体积/mL | 30% H2O2 的体积/mL | H2O 的体积/mL |
| 1 | 0.5 | 15 | 24.5mL |
| 2 | 0.5 | 30 | 9.5 |
 N2O4(g),也是放热反应,升温使平衡向左移动,C(NO2)增大,颜色加深.
N2O4(g),也是放热反应,升温使平衡向左移动,C(NO2)增大,颜色加深.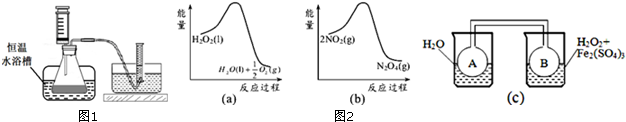
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
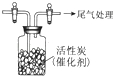 某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.
某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素的最简单气态氢化物中W的沸点最高 | |
| B. | W、X、Y、Z的简单阴离子都会促进水的电离 | |
| C. | 原子的半径:Y>Z>W>X | |
| D. | YX2、YX3通入BaCl2溶液中均有白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com