
(1)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式
(2)工业上常用铝热反应产生的“铁水”来焊接铁轨,请写出铝热反应的化学方程式
(3)冶金工业中,常用焦炭来冶炼铁。写出赤铁矿(Fe2O3)被CO还原成铁的化学方程式
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.醋酸钠的水解反应CH3COO-+H3O+===CH3COOH+H2O
B.碳酸氢钙与少量的NaOH溶液反应Ca2++2HCO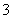 +2OH-===CaCO3↓+2H2O+CO
+2OH-===CaCO3↓+2H2O+CO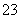
C.向AgCl悬浊液中滴加NaI溶液AgCl(s)+I-(aq)===AgI(s)+Cl-(aq)
D.稀硝酸与过量的铁屑反应Fe+4H++NO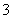 ===Fe3++NO↑+2H2O
===Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)===Si(s)+4HCl(g)
ΔH=+Q kJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器中进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol·L-1,则H2的反应速率为0.03 mol·L-1·min-1
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液中恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
关于元素周期表的下列叙述,错误的是 ( )
A.元素周期表揭示了化学元素的内在联系,是化学发展史上的重要里程碑之一
B.在周期表中,把电子层数相同的元素排成一横行,称为一周期
C.元素周期表中,总共有18个纵行,18个族
D.第IA族的元素又称为碱金属(除了H),第VIIA族的元素又称为卤素
查看答案和解析>>
科目:高中化学 来源: 题型:
海水淡化是指除去海水中的盐分以获得淡水的工艺过程,其方法较多,如反渗透法、电渗析法、离子交换法等,下列方法中也是用来进行海水淡化的是 ( )
A.过滤法 B. 萃取法 C.分液法 D.蒸馏法
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.元素性质随原子序数的递增呈周期性变化的根本原因是元素化合价呈周期性变化
B.核外电子根据其能量的差别处于不同的电子层,电子能量越高离核越近
C.所有原子的原子核都是由质子和中子构成的
D.在元素周期表中,具有相同电子层数的元素原子所处的周期序数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值。下列判断正确的是
A.28g N2含有的氮原子数目为NA
B.常温常压下,22.4L Cl2含有的分子数目为NA
C.1molNa变为Na+时失去的电子数目为NA
D.1L 1mol·L—1K2CO3溶液中含有的钾离子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
B.淀粉和纤维素都可以作为工业上生产葡萄糖的原料
C.油脂的水解反应,都是皂化反应
D.蔗糖是高分子化合物,其水解产物能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而
且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2 NaClO3 + 4 HCl=2 ClO2↑+ Cl2↑+ 2 NaCl + 2 H2O
方法二:2 NaClO3 + H2O2 + H2SO4=2 ClO2↑+ O2↑+Na2SO4 + 2 H2O
(1)方法一的离子方程式是 。
(2)方法二中被还原的物质是 ,若反应中产生的ClO2气体在标准状况下的体积为2.24L,则电子转移数为 NA。
(3)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:1,则Cl2与NaOH溶液反应时被还原的氯原子与被氧化的氯原子的物质的量之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com