
下列各组离子,在溶液中可以大量共存的是( )
A. H+ 、K+ 、CO32- 、SO42- B. Na+ 、OH- 、NH4+ 、 Cl-
C. Fe3+ 、Na+ 、OH- 、NO3- D.K+ 、Al3+ 、Cl- 、SO42-
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高二上期中文化学卷(解析版) 题型:选择题
滥用药物有碍健康,下列有关用药的叙述正确的是
A.长期大量服用阿司匹林可预防感冒
B.运动员长期服用麻黄碱可提高成绩
C.服用氢氧化钠溶液可中和过多的胃酸
D.注射青霉素前要先做皮肤敏感试验
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第二次月考化学试卷(解析版) 题型:选择题
一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:
c(Na+)+c(H+)=c(OH-)+c(HC2O4-)
D.pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:填空题
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾晶体)为翠绿色晶体,溶于水,难溶于乙醇,110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。
实验室利用(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:

已知:沉淀: FeC2O4·2H2O既难溶于水又难溶于强酸
6FeC2O4+3H2O2+6K2C2O4 4K3[Fe(C2O4)3]+2Fe(OH)3↓
4K3[Fe(C2O4)3]+2Fe(OH)3↓
2Fe(OH)3+3H2C2O4+3K2C2O4 2K3[Fe(C2O4)3]+6H2O
2K3[Fe(C2O4)3]+6H2O
(1)检验硫酸亚铁铵是否变质的试剂是 ;溶解时加几滴稀硫酸的目的是 。
(2)沉淀过滤后,洗涤1的操作方法是 。
(3)在沉淀中加入饱和K2C2O4溶液,并用40 ℃ 左右水浴加热,再向其中慢慢滴加足量的30%H2O2溶液,不断搅拌。此过程需保持温度在40 ℃ 左右,可能的原因是 。加入30%过氧化氢溶液完全反应后,煮沸的目的是 。
(4)洗涤2中所用洗涤试剂最合适的是 (填选项字母)。
A.草酸钠溶液 B.蒸馏水 C.乙醇 D.KCl溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试文化学试卷(解析版) 题型:填空题
某有机物的化学式为 C2H4O2,能与碳酸钠反应放出二氧化碳,则该有机物的结构简式是为 ,官能团的名称是_ _。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试理化学试卷(解析版) 题型:选择题
用2-丙醇为有机原料制取1,2-丙二醇,其各步反应所属的反应类型是
A.氧化→加成→水解 B.消去→加成→水解
C.水解→消去→加成 D.取代→水解→还原
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东深圳高级中学高一上期中考试化学试卷(解析版) 题型:选择题
欲配制下列四种无色透明的酸性溶液,其中能配制成功的是( )
A.NH4+、NO3-、Al3+、Cl- B.Na+、CH3COO-、K+、NO3-
C.MnO4-、K+、SO42-、Na+ D.Ca2+、Mg2+、HCO3-、CO32-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不 正确的是( )
正确的是( )
A.淀粉 葡萄糖
葡萄糖 CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B.维生素 葡萄糖
葡萄糖 CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C.油脂 甘油和高级脂肪酸
甘油和高级脂肪酸 CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D.蛋白质 氨基酸
氨基酸 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:填空题
300℃下,将2 mol SO2 1 mol O2混合于2 L的恒容密闭容器中,发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH,2分钟末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:
2SO3(g) ΔH,2分钟末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:
(1)能证明反应已经达到平 衡状态的是
衡状态的是
①c(SO2):c(O2):c(SO3)=2:1:2
②单位时间内生成nmol SO3的同时消耗nmol SO2
③反应速率2v(SO3)= v(O2)
④温度和体积一定时,容器内压强不再变化
⑤温度和压强一定时,混合气体的密度不再变化
(2)如图表示该反应的速率(v)随时间(t)的变化的关系:
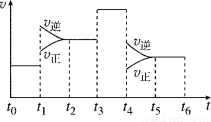
据图分析:你认为t3时改变的外界条件可能是________;t6时保持体积不变向体系中充入少量He气,平衡 移动。(填“向左”“向右”或“不”)。SO2%含量最高的区间是
(t0~t1,t2~t3,t3~t4,t5~t6)。
(3) 300℃时,该反应的平衡常数为 ,若升高温度该反应的平衡常数减小,则ΔH 0(填“大于”小于“或“不确定”)
(4)如果在相同条件下,上述反应从逆反应方向进行,开始时加入SO20.6 mol加入SO31.4 mol,若使平衡时各物质的量浓度与原来平衡相同,则还应加入O2 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com